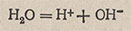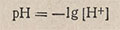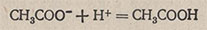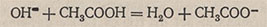- рН-метр. Как правильно откалибровать pH-метр
- Приготовление буферного раствора с точностью +/- 0.005 рН, измерение рН буферным раствором
- Изоэлектрическая точка электродов
- Настройка калибровки рН-метра изоэлектрической (опорной) точки (рН7), другой для настройки наклона (рН4/10)
- Измерение значение мВ в буфере рН=7 и рН=4, буферные растворы
- Значения мВ в буфере рН=7 и рН=4, пример:
- Проблема термокомпенсации, автоматическая термокомпенсация
- 1) Калибровка ph метра по буферу рН=7, теоретический наклон калибровочной кривой изменяется с температурой
- Компенсирование изменения наклона калибровочной прямой
- 2) Компенсация изменений равновесных концентраций ионов водорода в образцах с изменением температуры
- pH-Метрия
- Понятие pH
- Буферные растворы
- Буферные растворы по Зеренсену
- Измерение pH
рН-метр. Как правильно откалибровать pH-метр
Современный измерительный инструмент — электронный лабораторный прибор — рН-метр.
Особенности правильной калибровки pH-метров, настройка измерительного прибора для проведения точного измерения водородного показателя (показателя pH) водных растворов. рН-электроды — это не идеальные системы. Они могут иметь различную длину, несовершенную геометрическую форму, нарушения в составе внутреннего электролита и т.д.
Все это влияет на их характеристики и, в тоже время, это вполне нормально, так как в любом производстве существуют определенные допуски. Поэтому каждый рН-метр нуждается в калибровке, которая помогает прибору установить соотношение между сигналом от электрода и значением рН в растворе.
Калибровка pH-метра, настройка измерительного прибора для проведения точного измерения водородного показателя
Калибровка – очень ответственный момент! Надо отдавать себе отчет о невозможности измерения рН с точностью большей, чем используемые стандарты. Если работаете с точностью 0.01рН, то необходимо выполнение следующих условий: суммарная погрешность рН-метра и электрода не должна превышать 0.005 рН и проводить калибровку следует с особым вниманием на специальных высокоточных буферных растворах. Купить такие растворы нельзя, поскольку они не хранятся. Их придется готовить самостоятельно, с использованием специально подготовленных химических реактивов и воды.
Высокоточное измерение рН буферным раствором. Как приготовить буферный раствор с высокой точностью +/- 0.005 рН,
Приготовление буферного раствора с точностью +/- 0.005 рН, измерение рН буферным раствором
Если у Вас нет возможности приготовить буфер с точностью +/- 0.005 рН, то придется довольствоваться фирменными буферными растворами, точность которых обеспечивается на уровне +/- 0.02рН. При калибровке по таким стандартам суммарная погрешность не будет превышать 0.04 – 0.03 рН, при условии, что погрешность прибора находится на уроне 0.01 рН. Это самая распространенная практика, и Вы не найдете ни одной методики или ГОСТа, где требовалась бы поддержание рН с точностью выше, чем 0.05 рН. Исключение составляют лишь некоторые фармацевтические и специализированные производства.
Современные рН-электроды как правило комбинированные, т.е. в одном корпусе находятся и рН-электрод, и электрод сравнения.
Помимо удобства в работе, это обеспечивает более быстрый отклик и снижает суммарную ошибку.
Изоэлектрическая точка электродов
Изоэлектрическая точка для таких электродов находится на рН=7 (0 мВ). Поэтому, в первую очередь, прибор следует калибровать по буферу с нейтральным рН (например, 6.86 или 7.01). Вторую точку следует выбирать на расстоянии примерно 3 единицы рН, т.е. рН=4 или 10. Если прибор калибруется только по двум буферам, то выбор второй точки зависит от диапазона, в котором Вы преимущественно работаете.
Если это щелочные растворы, то воспользуйтесь буфером с рН=10, если кислые – с рН=4. Это связанно с некоторой разницей в наклонах калибровочных прямых в кислой и щелочной области. Проблем не возникнет, если Ваш прибор может калиброваться по трем и более точкам. В этом случае порядок калибровки не важен, так как рН-метр самостоятельно его отслеживает.
Настройка калибровки рН-метра изоэлектрической (опорной) точки (рН7), другой для настройки наклона (рН4/10)
На недорогих моделях рН-метров (HI8314, Piccolo, Checker) для калибровки предусмотрены два винта: один для настройки изоэлектрической (опорной) точки (рН7), другой для настройки наклона (рН4/10). Очень часто при использовании их путают, и возникает ситуация, когда взаимное положение винтов не позволяет провести калибровку.
В этом случае, перед проведением калибровки следует выставить оба винта в среднее положение (1/2 оборота для Piccolo и 15-16 оборотов для остальных моделей от крайнего положения).
Наиболее совершенные модели рН-метров имеют т.н. поддержку GLP, которая помимо даты последней калибровки позволяет оценить состояние электрода на основании данных об отношении наклона калибровочной кривой к теоретическому значению (59.16 при 25С) в %.
Измерение значение мВ в буфере рН=7 и рН=4, буферные растворы
Если у прибора нет поддержки GLP , но имеется режим измерения мВ, то наклон можно рассчитать самостоятельно, измерив значение мВ в буфере рН=7 и рН=4.
Значения мВ в буфере рН=7 и рН=4, пример:
| pH7 = -10 мВ | ||
| pH4 = +150 мВ | ||
| наклон = 150 – (-10)/59.2х3 = 90.1% | ||
| 95 – 102% | электрод в рабочем состоянии | the electrode is in working condition |
| 92 – 95% | электрод нуждается в очистке | the electrode needs cleaning |
| менее 92% | необходимо сменить электролит или заменить электрод | it is necessary to change the electrolyte or replace the electrode. |
Проблема термокомпенсации, автоматическая термокомпенсация
Проблема компенсации изменений температуры одна из самых важных и самых трудно решаемых в рН-метрии.
Погрешность в измерения возникает по трем причинам:
| 1) | В уравнение Нернста входит температура; | The Nernst equation includes temperature; |
| 2) | Равновесные концентрации ионов водорода в буфере и образцах меняются в зависимости от температуры; | he equilibrium concentrations of hydrogen ions in the buffer and samples vary with temperature; |
| 3) | Характеристики рН-электрода зависят от температуры. | The characteristics of the pH electrode depend on the temperature. |
1) Калибровка ph метра по буферу рН=7, теоретический наклон калибровочной кривой изменяется с температурой
1. Согласно уравнению Нернста, теоретический наклон калибровочной кривой изменяется с температурой. Если прибор не учитывает этого изменения, то к погрешности измерений добавляется ошибка в среднем равная 0.003рН на каждый градус Цельсия и каждую единицу рН от изопотенциальной точки.
Например: прибор откалиброван по буферу рН=7 при температуре 25 С.
| Образец с рН=5 | при 20С | ошибка = 0.003 х 5 х 2 = 0.03 |
| Образец с рН=2.5 | при 2С | ошибка = 0.003 х 23 х 4.5 = 0.31 |
| Образец с рН=12 | при 80С | ошибка = 0.003 х 55 х 5 = 0.82 |
Компенсирование изменения наклона калибровочной прямой
Компенсировать изменение наклона калибровочной прямой очень просто, поэтому это делает практически любой современный рН-метр, за исключением самых простейших. Это то, что в рекламных проспектах и спецификациях называется «автоматической термокомпенсацией» (автотермокоменсация, АТС, ATC). Но ни один из приборов не позволяет учитывать следующие две составляющие погрешности.
2) Компенсация изменений равновесных концентраций ионов водорода в образцах с изменением температуры
2. Гораздо более сложной задачей является компенсация изменений равновесных концентраций ионов водорода в образцах с изменением температуры. Проблема заключается в том, что не зная точного химического состава образца невозможно предсказать характер этих изменений.
Существует только общая закономерность, что рН нейтральных и щелочных растворов сильнее зависит от изменения температуры, чем рН кислых растворов.
При изменении температуры на 25-30 градусов рН может измениться на 0.5 – 1 единицы.
Обычные общелабораторные рН-метры никак не учитывают этот фактор, да его и невозможно учесть, так как растворы бывают самые разные. Исключения не составляют и буферные растворы:
Источник
pH-Метрия
Понятие pH
Вода является слабым электролитом; она слабо диссоциирует по уравнению
При 25 °С в 1 л воды распадается на ионы 10-7 моль H2O. Концентрация ионов H+ и OH- (в моль/л) будет равна
Чистая вода имеет нейтральную реакцию. При добавлении в нее кислоты концентрация ионов H+ увеличивается, т.е. [H+] > 10-7 моль/л; концентрация ионов OH- уменьшается, т.е. [OH-] меньше 10-7 моль/л. При добавлении щелочи концентрация ионов OH- увеличивается: [OH-] > 10-7 моль/л, следовательно, [H+] меньше 10-7 моль/л.
На практике для выражения кислотности или щелочности раствора вместо концентрации [H+] используют ее отрицательный десятичный логарифм, который называют водородным показателем pH:
В нейтральной воде pH = 7. Значения pH и соответствующие им концентрации ионов H+ и OH- приведены в табл. 4.
Буферные растворы
Многие аналитические реакции проводят при строго определенном значении pH, которое должно сохраниться в течение всего времени проведения реакции. В ходе некоторых реакций pH может изменяться в результате связывания или высвобождения ионов H+. Для сохранения постоянного значения pH применяют буферные растворы.
Буферные растворы представляют собой чаще всего смеси слабых кислот с солями этих кислот или смеси слабых оснований с солями этих же оснований. Если, например, в ацетатный буферный раствор, состоящий из уксусной кислоты CH3COOH и ацетата натрия CH3COONa добавить некоторое количество такой сильной кислоты, как HCl, она будет реагировать с ацетат-ионами с образованием малодиссоциирующей CH3COOH:
Таким образом, добавленные в раствор ионы H+ не останутся свободными, а будут связаны ионами CH3COO-, и поэтому pH раствора почти не изменится. При добавлении раствора щелочи к ацетатному буферному раствору ионы OH- будут связаны недиссоциированными молекулами уксусной кислоты CH3COOH:
Следовательно, pH раствора и в этом случае также почти не изменится.
Буферные растворы сохраняют свое буферное действие до определенного предела, т.е. они обладают определенной буферной емкостью. Если ионов H+ или OH- оказалось в растворе больше, чем позволяет буферная емкость раствора, то pH будет изменяться в значительной степени, как и в небуферном растворе.
Обычно в методиках анализа указывается, каким именно буферным раствором следует пользоваться при выполнении данного анализа и как его следует приготовить. Буферные смеси с точным значением pH выпускают в виде фиксаналов в ампулах для приготовления 500 мл раствора.
pH = 1,00. Состав: 0,084 г гликокола (аминоуксусной кислоты NH2CH2COOH), 0,066 г хлорида натрия NaCl и 2,228 г соляной кислоты HCl.
pH = 2,00. Состав: 3,215 г лимонной кислоты C6H8O7-H2O, 1,224 г гидроксида натрия NaOH и 1,265 г соляной кислоты HCl.
pH = 3,00. Состав: 4,235 г лимонной кислоты C6H8O7-H2O, 1,612 г гидроксида натрия NaOH и 1,088 г соляной кислоты HCl.
pH = 4,00. Состав: 5,884 г лимонной кислоты C6H8O7-H2O, 2,240 г гидроксида натрия NaOH и 0,802 г соляной кислоты HCl.
pH = 5,00. Состав: 10,128 г лимонной кислоты C6H8O7-H2O и 3,920 г гидроксида натрия NaOH.
pH = 6,00. Состав: 6,263 г лимонной кислоты C6H8O7-H2O и 3,160 г гидроксида натрия NaOH.
pH = 7,00. Состав: 1,761 г дигидрофосфата калия KH2PO4 и 3,6325 г гидрофосфата натрия Na2HPO4-2H2O.
pH = 8,00. Состав: 3,464 г борной кислоты H3BO3, 1,117 г гидроксида натрия NaOH и 0,805 г соляной кислоты HCl.
pH = 9,00. Состав: 1,546 г борной кислоты H3BO3, 1,864 г хлорида калия, KCl и 0,426 г гидроксида натрия NaOH.
pH = 10,00. Состав: 1,546 г борной кислоты H3BO3, 1,864 г хлорида калия KCl и 0,878 г гидроксида натрия NaOH.
pH = 11,00. Состав: 2,225 г гидрофосфата натрия Na2HPO4-2H2O и 0,068 г гидроксида натрия NaOH.
pH = 12,00. Состав: 2,225 г гидрофосфата натрия Na2HPO4-2H2O и 0,446 г гидроксида натрия NaOH.
pH = 13,00. Состав: 1,864 г хлорида калия KCl и 0,942 г гидроксида натрия NaOH.
Отклонения от номинального значения pH достигают ±0,02 для растворов при pH от 1 до 10 и ±0,05 при pH от 11 до 13. Такая точность вполне достаточна для практических работ.
Для настройки pH-метров применяют стандартные буферные растворы с точными значениями pH.
1. Ацетатный буферный раствор с pH=4,62: 6,005 г уксусной кислоты CH3COOH и 8,204 г ацетата натрия CH3COONa в 1 л раствора.
2. Фосфатный буферный раствор с pH=6,88: 4,450 г гидрофосфата натрия Na2HPO4-2H2O и 3,400 г дигидрофосфата калия KH2PO4 в 1 л раствора.
3. Боратный буферный раствор с pH=9,22: 3,81 г тетрабората натрия Na2B4O7-10H2O в 1 л раствора.
4. Фосфатный буферный раствор с pH=11,00: 4,450 г гидрофосфата натрия Na2HPO4-2H2O и 0,136 г гидроксида натрия NaOH в 1 л раствора.
Буферные растворы по Зеренсену
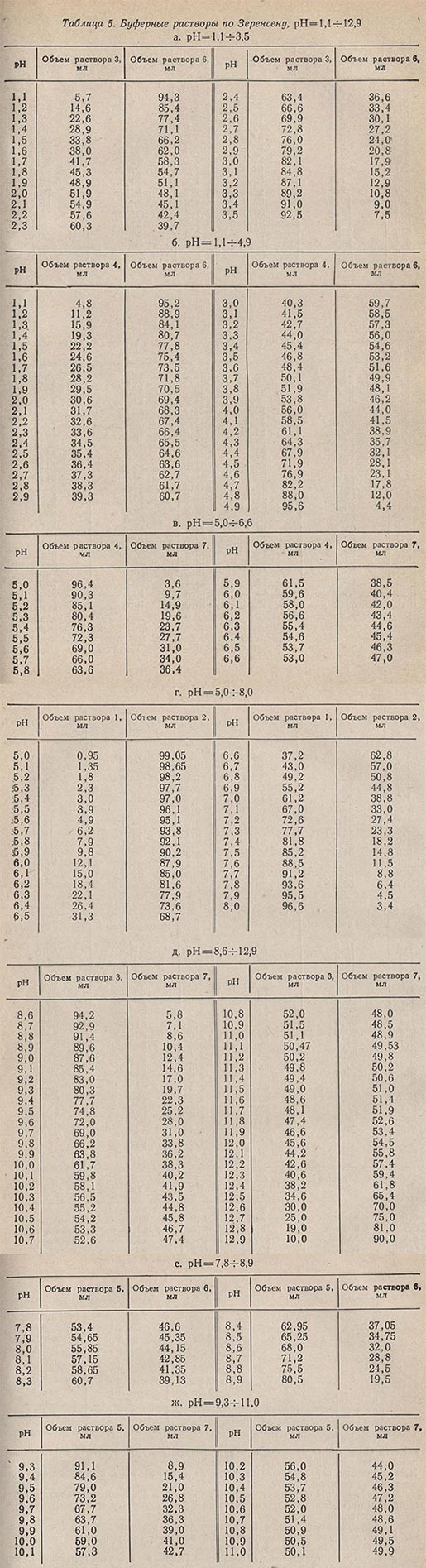
Для приготовления буферных растворов для агрохимического и биохимического анализа со значениями pH от 1,1 до 12,9 с интервалом в 0,1 применяют 7 основных исходных растворов.
Раствор 1. Растворяют 11,866 г гидрофосфата натрия Na2HPO4-2H2O в воде и разбавляют в мерной колбе водой до 1 л (концентрация раствора 1/15 М).
Раствор 2. Растворяют 9,073 дигидрофосфата калия KH2PO4 в 1 л воды в мерной колбе (концентрация 1/15 М).
Раствор 3. Растворяют 7,507 г гликокола (аминоуксусной кислоты) NH2CH2COOH и 5,84 г хлорида натрия NaCl в 1 л воды в мерной колбе. Из этого раствора путем смешивания с 0,1 н. раствором HCl готовят буферные растворы с pH от 1,1 до 3,5; смешиванием с 0,1 н. раствором NaOH готовят растворы с pH от 8,6 до 12,9.
Раствор 4. Растворяют 21,014 г лимонной кислоты C6H8O7-H2O в воде, добавляют к раствору 200 мл 1 н. раствора NaOH и разбавляют до 1 л водой в мерной колбе. Смешиванием этого раствора с 0,1 н. раствором HCl готовят буферные растворы с pH от 1,1 до 4,9; смешиванием с 0,1 н. раствором NaOH готовят буферные растворы с pH от 5,0 до 6,6.
Раствор 5. Растворяют 12,367 г борной кислоты H3BO3 в воде, добавляют 100 мл 1 н. раствора NaOH и разбавляют водой до 1 л в мерной колбе. Смешиванием этого раствора с 0,1 н. раствором HCl готовят буферные растворы с pH от 7,8 до 8,9; смешиванием с 0,1 н. раствором NaOH готовят буферные растворы с рН от 9,3 до 11,0.
Раствор 6. Готовят точно 0,1 н. раствор HCl;
Раствор 7. Готовят точно 0,1 н. раствор NaOH; дистиллированную воду для приготовления раствора кипятят 2 ч для удаления CO2. Раствор при хранении защищают от попадания CO2 из воздуха хлоркальциевой трубкой.
В некоторых растворах при хранении образуется налет плесени, для предотвращения этого к раствору прибавляют несколько капель тимола в качестве консервирующего средства. Для приготовления буферного раствора требуемого pH смешивают указанные растворы в определенном соотношении (табл. 5). Объем измеряют с помощью бюретки вместимостью 100,0 мл. Все значения pH буферных растворов в таблице приведены к температуре 20 °С.
Для приготовления исходных растворов используют реактивы квалификации хч. Гидрофосфат натрия Na2HPO4-2H2O предварительно дважды перекристаллизовывают. При второй перекристаллизации температура раствора не должна превышать 90 °С. Полученный препарат слегка увлажняют и высушивают в термостате при 36 °С в течение двух суток. Дигидрофосфат калия KH2PO4 также дважды перекристаллизовывают и высушивают при 110-120 °С. Хлорид натрия NaCl дважды перекристаллизовывают и сушат при 120 °С. Лимонную кислоту C6H8O7-H2O дважды перекристаллизовывают. При второй перекристаллизации температура раствора не должна быть выше 60 °С. Борную кислоту H3BO3 дважды перекристаллизовывают из кипящей воды и высушивают при температуре не выше 80 °С.
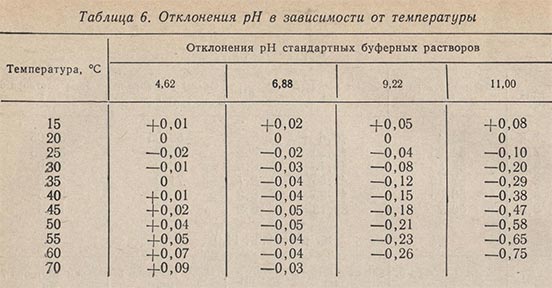
На значение pH оказывает влияние температура буферного раствора. В табл. 6 приведены отклонения pH в зависимости от температуры стандартных буферных растворов.
Для создания заданного pH в анализируемом растворе при комплексометрических титрованиях применяют буферные растворы следующего состава.
pH = 1. Соляная кислота, 0,1 н. раствор.
pH = 2. Смесь гликокола NH2-CH2-COOH и его солянокислой соли NH2-CH2-COOH-HCl. Твердый гликокол (0,2-0,3 г) прибавляют к 100 мл солянокислого раствора соли.
pH = 4-6,5. Ацетатная смесь 1 н. раствора ацетата натрия и 1 н. раствора уксусной кислоты. Растворы смешивают перед применением в равных объемах.
pH = 5. Смесь раствора 27,22 г кристаллического ацетата натрия и 60 мл 1 н. раствора HCl разбавляют до 1 л водой.
pH = 5,5. Ацетатная смесь. Растворяют 540 г ацетата натрия в воде и разбавляют до 1 л. К полученному раствору добавляют 500 мл 1 н. раствора уксусной кислоты.
pH = 6,5-8. Триэтаноламин и его солянокислая соль. Смешивают 1 М раствор триэтаноламина N(C2H4OH)3 и 1 М раствор HCl в равных объемах перед применением.
pH = 8,5-9,0. Аммиачно-ацетатная смесь. К 500 мл концентрированного аммиака добавляют 300 мл ледяной уксусной кислоты и разбавляют водой до 1 л.
pH = 9. Боратная смесь. Смешивают 100 мл 0,3 М раствора борной кислоты с 45 мл 0,5 н. раствора едкого натра.
pH = 8-11. Аммиак — хлорид аммония. Смешивают 1 н. раствор NH4OH и 1 н. раствор NH4Cl в равных объемах перед применением.
pH = 10. К 570 мл концентрированного раствора аммиака прибавляют 70 г хлорида аммония и разбавляют водой до 1 л.
рН = 11-13. Едкий натр, 0,1 н. раствор.
При комплексометрическом определении общей жесткости воды применяют буферные таблетки серо-бурого цвета, приготовленные совместно с индикатором (эриохром черный Т). К пробе воды (100 мл) достаточно добавить несколько капель раствора сульфида натрия (для маскировки тяжелых металлов), две буферные таблетки и 1 мл концентрированного аммиака. После растворения таблеток раствор окрашивается в красный цвет; его оттитровывают 0,02 М раствором ЭДТА до устойчивого зеленого окрашивания. 1 мл 0,02 М раствора ЭДТА соответствует 0,02 экв/л жесткости воды. Выпускаются в ГДР.
Измерение pH
Для определения pH растворов применяют специальные реактивы — индикаторы, а также приборы — pH-метры (электрометрическое определение pH).
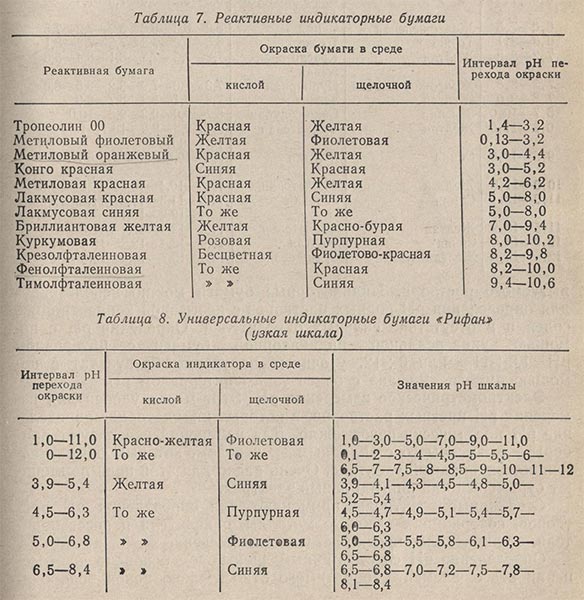
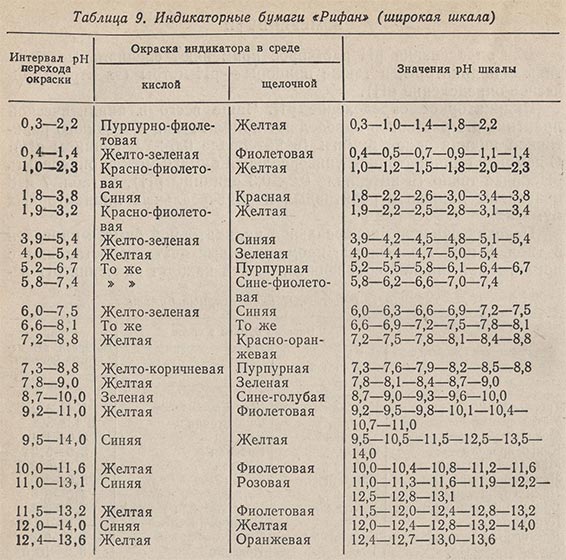
Индикаторное определение pH. Чаще всего в аналитической практике pH растворов определяют приближенно с помощью реактивной индикаторной бумаги (в интервале 0,5-2,0 единицы pH). С помощью индикаторной универсальной бумаги можно определить pH более точно (в интервале 0,2-0,3 единицы pH). В табл. 7 и 8 приведены данные о реактивных и универсальных индикаторных бумагах.
Переход окраски универсальной индикаторной бумаги приведен в табл. 8 и 9. Полученные промежуточные цвета сопоставляют с прилагаемой шкалой сравнения и по ней находят значения pH испытуемого раствора. Индикаторные бумаги можно использовать для определения pH водных растворов с невысокой концентрацией солей и в отсутствие сильных окислителей. Определив pH с помощью универсальной индикаторной бумаги с интервалом pH = 1,0-11,0 или 0-12, уточняют полученный результат с помощью бумаги «Рифан» с более узким интервалом pH.
Электрометрическое измерение pH. Этот метод удобен для измерения pH цветных растворов, в которых индикаторное определение pH (пш) практически невозможно. Для измерений используют приборы — pH-метры со стеклянным электродом, которым обычно заменяют водородный электрод. Очень редко для этой цели применяют сурьмяный или хингидронный электрод.
Стеклянные электроды применяют для определения pH растворов, содержащих тяжелые металлы, окислители и восстановители, а также коллоидных растворов и эмульсий. Определение pH со стеклянным электродом основано на изменении э.д.с. элемента, обратимого относительно ионов водорода.
Потенциал поверхности стекла, соприкасающегося с раствором кислоты, зависит от pH раствора. Это свойство стекла использовано в стеклянных электродах — индикаторах pH. Стеклянный электрод обычно имеет форму пробирки, донная часть которой выполнена в виде тонкостенной стеклянной пластинки или в виде шарика с толщиной стенок не более 0,01 мм. В стеклянный электрод наливают буферный раствор с известным pH и помещают в исследуемый раствор.
В качестве электрода сравнения используют каломельный электрод. Этот электрод представляет собой сосуд, на дне которого находится ртуть, соединенная с цепью платиновой проволокой. Над ртутью находится каломельная паста с кристаллами KCl, сверху насыщенные растворы KCl и каломели (Hg2Cl2). Контакт электрода с исследуемым раствором происходит через тонкое асбестовое волокно. Каломельный электрод сравнения можно применять для измерений pH при температуре не выше 60 °С; нельзя измерять pH растворов, содержащих фториды.
Прибор pH-метр проверяют и настраивают всегда по тому буферному раствору, pH которого близок к pH исследуемого раствора. Например, для измерения pH в области от 2 до 6 готовят буферный раствор по Зеренсену с pH = 3 или 4 или применяют стандартный буферный раствор с pH = 4,62.
В лабораторной практике для измерения pH применяют pH-метр ЛПУ-01, который предназначен для определения pH растворов в пределах от -2 до 14 с диапазоном через 4 единицы pH: -2-2; 2-4; 6-10; 10-14. Чувствительность прибора — 0,01 pH. Используют также pH-метр лабораторный специальный ЛПС-02; pH-метр типа ПЛ-У1 и переносной pH-метр-милливольтметр ППМ-03М1.
Промышленным преобразователем повышенной точности является pH-метр типа pH-261, который предназначается для измерений pH растворов и пульп. В полевых условиях для измерений pH водных растворов применяют pH-метр pH-47М; для измерений pH солевых почвенных вытяжек — pH-метр ПЛП-64; для молока и молочных продуктов применяют pH-метр pH-222-2. Работа на pH-метрах осуществляется согласно инструкции, прилагаемой к каждому прибору.
Источник