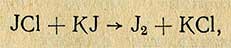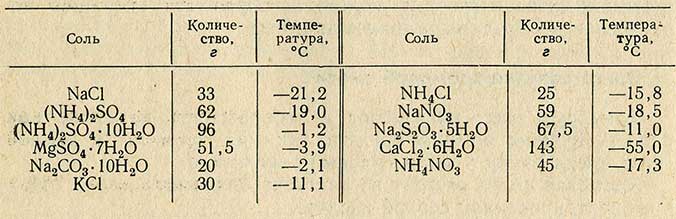- Хромовая смесь
- Состав и приготовление хромовой смеси
- Химические методы очистки посуды
- Глава 7. Практические указания
- Очистка (возгонка) йода
- Приготовление хромовой смеси
- Приготовление охлаждающих смесей
- Нанесение огнестойких надписей на фарфор
- Приготовление абсолютного этилового спирта
- Определение концентрации перекиси водорода
- Очистка перекиси водорода от примесей серной кислоты
- Очистка этилового эфира от перекисей
- Проверка термометров
Хромовая смесь
Хромовая смесь — смесь концентрированной серной кислоты и дихромата калия; при действии серной кислоты на бихромат образуется хромовый ангидрид CrO3.
Хромовая смесь является одним из сильнейших окислителей. Широко используется в лабораторной технике для мытья стеклянной химической посуды, а также применяется в отбеливающем процессе обращаемой фотографии.
Состав и приготовление хромовой смеси
Существует много рецептур этого распространённого лабораторного препарата.
- Состав 1:
Дихромат калия — 60 г Концентрированная серная кислота — 80 мл Вода — 270 мл
- Состав 2:
Дихромат калия — 15 г Концентрированная серная кислота — 500 мл
- Состав 3:
Дихромат калия — 50 г Концентрированная серная кислота — 1 л Состав 4: Дихромат калия — 10 г Концентрированная серная кислота — 100 мл Вода — 10-20 мл (если при приготовлении хромпика было добавлено много воды, то из раствора выпадает оранжевый осадок, чтобы его растворить необходимо добавить дополнительное количество серной кислоты)
Для приготовления хромовой смеси растворяют в тёплой воде дихромат калия, раствор охлаждают, и затем осторожно при перемешивании добавляют серную кислоту (добавлять кислоту в водный раствор дихромата, но не наоборот!). Смесь сильно нагревается, а раствор приобретает тёмно-коричневый цвет.
Стеклянную посуду выдерживают в хромовой смеси несколько минут, при необходимости — пару дней, а затем тщательно промывают в проточной воде. На хорошо обезжиренном стекле вода растекается тонким слоем, не собираясь в капли.
В результате протекающих реакций окисления органических веществ хромовый ангидрид восстанавливается до сульфата хрома(III), в результате чего использованная хромовая смесь постепенно изменяет цвет на зелёный.
Источник
Химические методы очистки посуды
Мытье хромовой смесью. Очень часто в лабораториях для мытья посуды применяют хромовую смесь, так как хромовокислые соли в кислом растворе являются сильными окислителями. Для приготовления хромовой смеси в концентрированную серную кислоту добавляют около 5% (от массы серной кислоты) размельченного в порошок кристаллического двухромовокислого калия и осторожно нагревают в фарфоровой чашке на водяной бане до растворения его.
Для приготовления хромовой смеси можно применять также двухромовокислый натрий, который растворяют в воде, а затем в раствор осторожно добавляют серную кислоту.
Смесь готовят из расчета:
Двухромовокислый натрий. 6 г
Серная кислота (1,84 г/мл) . 100 мл
При мытье хромовой смесью посуду споласкивают сначала водой, а потом наливают слегка подогретую хромовую смесь до 1/3 объема сосуда и осторожно и медленно смачивают внутренние стенкн его. После этого хромовую смесь выливают обратно в тот же со-, суд, в котором она хранится, причем стараются смочить ею оставшиеся не смоченными стенки посуды и особенно наиболее загрязненные ее края. Слив всю жидкость, посуду оставляют постоять несколько минут, затем ее моют сначала водопроводной водой (лучше теплой), потом дистиллированной. ‘
Сильно загрязненную посуду моют хромовой смесью несколько раз.
Труднее всего отмываются загрязнения на горлышках колб. Чтобы отмыть их, хромовую смесь наливают в стакан, опускают в него горло колбы, слегка обогретой (достаточно нагревания рукой), после того как колба охладится, жидкость несколько поднимается внутрь ее. Через одну-две минуты колбу вынимают, дают стечь хромовой смеси, а затем колбу моют водой, как описано выше.
Хромовая смесь служит довольно долго. После длительного употребления ее цвет из темио-оранжевого переходит в темно-зеленый, что служит признаком ее дальнейшей непригодности для мытья. В лаборатории всегда должен быть запас хромовой смеси *.
Хромовая смесь очень сильно действует на кожу и одежду, поэтому обращаться с ней следует осторожно.
Неопытные работники при мытье пипеток и трубок часто набирают хромовую смесь в них ртом. При этом

Рис. 167. Резиновая груша, надетая на пипетку.
Рис. 168. Мытье пипеток, бюреток и трубок в толстостенном цилиндре.
случается, что хромовая смесь засасывается в рот, вызывая ожоги полости рта и порчу зубов. Хромовую смесь следует набирать в пипетку при помощи резиновой груши без баллона (рис. 167). К груше присоединяют резиновую трубку, конец которой надевают на пипетку. Сжав рукой грушу, чтобы удалить из нее воздух, и закрыв большим пальцем отверстие для поступления воздуха, пипетку опускают в хромовую смесь. Постепенно разжимают руку (большой палец с отверстия не снимать), вну-
* Хромовую смесь иногда готовят из разбавленной серной кислоты, но в этом случае она менее эффективна.
три пипетки образуется разрежение и хромовая смесь поднимается в нее. Набрав полную пипетку и продержав в ней хромовую смесь 1—2 мин, отнимают большой палец от отверстия груши и дают жидкости стечь.
Повторив несколько раз эту операцию, пипетку моют, как обычно.
Пипетки, бюретки и подобные им длинные трубки удобно также мыть хромовой смесью в толстостенном цилиндре такой высоты, чтобы трубки могли быть погружены в него более чем на половину. В цилиндр помещают подлежащие мытью трубки и заливают его почти доверху хромовой смесью. Через некоторое время трубки вынимают и помещают их в цилиндр обратными концами (рис. 168).
В качестве моющего средства можно применять также раствор К2Сr2О7 в концентрированной HNO3. Для приготовления этого раствора 200 г К2Сr2О7 растворяют в 1 л HNO3. Такой раствор даже при комнатной температуре по своим моющим свойствам превосходит хромовую смесь и устойчив в течение длительного времени.
Хромовую- смесь не применяют, если посуда загрязнена парафином, керосином, воском, минеральными маслами и вообще продуктами перегонки нефти. В этих случаях посуду моют паром или органическими растворителями.
Нужно избегать попадания в хромовую смесь спиртов— этилового или метилового, тотчас окисляющихся и восстанавливающих Сr2О7 -ион до Cr3+. В результате этого раствор приобретает зеленую окраску и делается непригодным для дальнейшего применения.
Если посуда загрязнена солями бария, мыть ее хромовой смесью, содержащей серную кислоту, нельзя, так как получающийся сернокислый барий образует на стенках посуды трудно удаляемый осадок.
Нужно заметить, что хромовую смесь полезно применять слегка подогретой (до 45—5O0C), тогда она действует сильнее.
Подогреть хромовую смесь можно по-разному:
1) отлив некоторое количество хромовой смеси в колбу, ее подогревают на горячей водяной бане;
2) осторожно добавляют в хромовую смесь немного воды и концентрированной серной кислоты;
3) можно также отмываемый предмет предварительно сполоснуть горячей водой.
Если хромовая смесь попадает на кожу рук или одежду, их следует прежде всего обмыть большим количеством воды, затем раствором соды (двууглекислого натрия) или аммиака.
Мытье марганцевокислым калием. Хорошим средством для мытья посуды является 4%-ный раствор марганцовокислого калия.
Раствор марганцевокислого калия — сильный окислитель, особенно когда он -подогрет и подкислен серной кислотой; его наливают в посуду, которую нужно предварительно вымыть горячей водой и вычистить ершом или щеткой. Затем тонкой струей добавляют немного концентрированной серной кислоты, что вызывает разогревание, вполне достаточное, чтобы все загрязнения на стенках быстро окислились. Серную кислоту следует брать в таком количестве, чтобы после добавления се температура раствора была около 50—60° С. Обычно на 100 мл раствора марганцевокислого калия бывает достаточно добавить 3—5 мл концентрированной серной кис-. лоты.
Нужно брать именно серную кислоту и ни в каком случае не соляную, так как последняя окисляется марганцевокислым калием с образованием свободного хлора.
Иногда после мытья посуды раствором марганцевокислого калия на стенках ее появляется бурый налет; его можно удалить, споласкивая посуду 5%-ным раствором кислого сернокислого натрия (NaHSO3), растворами закисного сернокислого железа (FeSO4), соли Мора или органических кислот, лучше всего щавелевой. После этого посуду моют водой.
При работе с подкисленным раствором марганцевокислого калия следует придерживаться тех же приемов мытья и мер предосторожности, которые описаны выше для хромовой смеси.
Отработанный подкисленный раствор марганцевокислого калия обычно выливают и повторно не используют. Если же применялся неподкисленный раствор, его можно использовать несколько раз.
Подкисленным раствором марганцевокислого калия очень хорошо очищаются ртутные насосы, трубки барометров и пр.
Иногда можно применять раствор марганцевокислого калия, в который добавляют какую-нибудь щелочь. Такой раствор является более мягким окислителем, и после мытья им стенки посуды покрываются бурым налетом двуокиси марганца, удаление которого проводится одним из приемов, описанных выше.
Мытье смесью соляной кислоты и перекиси водорода. Очень удобным и доступным окислителем, который с успехом можно применять для мытья химической посуды, является смесь Комаровского, состоящая из равных объемов 6 н. раствора HCI и 5—6%-ного раствора перекиси водорода. Эта смесь действует очень энергично, особенно при небольшом подогревании, при этом она не влияет па стекло, чего нельзя сказать о хромовой смеси или подкисленном растворе марганцовокислого калия. Вместо соляной кислоты можно пользоваться и уксусной.
Для мытья смесь наливают в слегка подогретую посуду (мерную посуду нагревать нельзя) или же подогревают смесь до 30—40° С. Обмывают стенки посуды смесью, затем выливают ее в ту же посуду, в которой она хранилась, для повторного использования. После этого посуду моют водой, как обычно.
Мытье серной кислотой и растворами щелочей. Когда посуда загрязнена смолистыми веществами, нерастворимыми в соде, а также в тех случаях, когда в лаборатории нет хромовой смеси, посуду можно мыть концентрированной серной кислотой или концентрированным (до 40%) раствором щелочи (NaOH, КОН). Смолы большей частью растворяются или в кислоте, или в щелочи. Загрязненный сосуд заполняют на 1Z4 щелочью (если смолы много, жидкость наливают так, чтобы вся смола была покрыта ею, ио сосуд можно было бы свободно встряхивать). Когда смолы много, операцию повторяют несколько раз.
Продолжительность обработки кислотой или щелочью зависит от особенностей смолы *. В одних случаях смолу, можно удалить, встряхивая колбу в течение 5—10 мин, в других же случаях приходится отмывать смолу в течение нескольких часов, периодически встряхивая колбу.
Обращаться с концентрированными серной кислотой и щелочью нужно осторожно; кислоту нельзя выливать в раковину. Загрязненную смолой серную кислоту или
* Растворимость смолы зависит or того, насколько далеко зашла термическая деструкция (пиролиз) органического соединения, из которого образовалась смола, и как много содержится в ней угля (свободного углерода).
щелочь следует сливать в глиняные или стеклянные банки, которые всегда должны стоять около водопроводной раковины. Сливать в одну банку кислоту и щелочь нельзя, так как при этом будет происходить нейтрализация, сопровождающаяся сильным разогреванием, вследствие чего содержимое банки может разбрызгиваться *.
Кроме растворов едких натра или кали, полезно пользоваться и менее сильными щелочами, например известковым молоком, что, в частности, очень удобно для мытья посуды, загрязненной керосином. Для этого в посуду наливают раствор известкового молока (5—10%) н энергично встряхивают. Повторяя операцию два-три раза, очищают посуду от следов керосина. Много известкового молока брать не следует. На колбу емкостью 1 л достаточно взять 100—200 мл.
После обработки известковым молоком посуду моют теплой водой **.
Источник
Глава 7. Практические указания
Очистка (возгонка) йода
Йод, имеющийся в продаже, содержит примеси JCl, JBr, JCl3 и воду, поэтому в лаборатории для получения химически чистого реактива йод очищают следующим образом.
К 16 частям (граммам) йода прибавляют две части йодистого калия и восемь частей прокаленной окиси кальция.
Йодистый калий вытесняет йод из его соединений с галоидами:
Окись кальция применяется для поглощения воды.
Навески йода, йодистого калия и окиси кальция высыпают в агатовую ступку, быстро растирают пестиком и переносят в колбу из жаростойкого стекла для возгонки. В колбу через пробку вставляют пробирку с холодной водой и, быстро вращая колбу на пламени горелки (обогревая только дно), возгоняют йод. Нагревают колбу до тех пор, пока весь объем колбы не заполнится парами йода, после этого колбу охлаждают на асбестовой сетке. При охлаждении пары йода конденсируются на холодной пробирке.
Кристаллы, образовавшиеся на стенках пробирки, снимают в бюкс и снова нагревают колбу, повторяя эту операцию до получения необходимого количества йода.
Приготовление хромовой смеси
Хромовую смесь применяют в лабораторной практике как одно из лучших моющих средств, так как хроматы в кислой среде представляют собой сильные окислители.
Хромовая смесь состоит из раствора бихромата калия (5%) в концентрированной серной кислоте.
Для приготовления берут 9,2 г растертого в порошок бихромата калия, переносят в фарфоровую чашку, приливают 100 мл концентрированной серной кислоты и нагревают на водяной бане при помешивании стеклянной палочкой до полного растворения K2Cr2O7.
Как моющее средство применяют также раствор бихромата натрия в разбавленной серной кислоте; 6 г Na2Cr2O7 растворяют в 100 мл воды и затем прибавляют 100 мл концентрированной серной кислоты.
Хромовую смесь применяют следующим образом: загрязненную посуду предварительно ополаскивают водой, затем наливают в нее 1/3 — 1/4 объема хромовой смеси и осторожными движениями смачивают внутренние стенки посуды.
После этого смесь сливают, посуду оставляют на несколько минут, а затем ее хорошо моют водопроводной водой и споласкивают дистиллированной водой.
Хромовую смесь не следует применять для мытья посуды, загрязненной парафином, воском, керосином, продуктами перегонки нефти, а также солями бария. На посуде, загрязненной солями бария, образуются труднорастворимые соли сульфата бария.
Хромовая смесь сильно разрушает растительные и животные ткани (одежду, обувь, кожу), поэтому при работе с ней необходимо соблюдать большую осторожность.
Приготовление охлаждающих смесей
Приготовление охлаждающих смесей основано на свойстве некоторых солей поглощать большое количество тепла при растворении в воде, в результате чего растворы этих солей имеют низкую температуру.
Применяя вместо воды лед или снег, получают еще более низкую температуру смеси.
При смешивании 100 г снега или мелко истолченного льда с солью в количествах, приведенных в табл. 8, получают охлаждающие смеси с пониженной температурой соответственно применяемой соли.
Нанесение огнестойких надписей на фарфор
а) Раствор хлорного железа в концентрированной соляной кислоте наносят очень тонким, едва заметным слоем на фарфоровую посуду, затем сушат и прокаливают.
б) К смеси, состоящей из двуокиси марганца — 10 весовых частей, окиси цинка — 10 весовых частей и буры — 1 весовой части и хорошо растертой в фарфоровй ступке, добавляют 21%-ный раствор силиката натрия до консистенции, при которой смесь можно наносить на фарфоровую посуду.
Приготовление абсолютного этилового спирта
При абсолютировании, или обезвоживании, спирт обрабатывают сернокислой медью (CuSO4) или окисью кальция (CaO).
Если применяют CuSO4, абсолютирование проводят следующим образом. К 1 л этилового спирта добавляют 200-500 г порошка свежепрокаленной и охлажденной в эксикаторе CuSO4 и кипятят с обратным холодильником в течение 6 ч.
После этого колбу с содержимым оставляют на ночь (закрыв пробкой с хлоркальциевой трубкой); на следующий день этиловый спирт сливают и дважды перегоняют с применением дефлегматора.
При обработке окисью кальция в колбу к 1 л этилового спирта добавляют 250 г обезвоженного CaO, закрывают колбу пробкой с хлоркальциевой трубкой и оставляют на 2 дня при периодическом перемешивании. После этого смесь для удаления альдегидов кипятят на водяной бане с обратным холодильником 30-40 мин; затем спирт перегоняют с применением дефлегматора.
После такой обработки этиловый спирт получают с содержанием 99,5% C2H5OH.
Более полное удаление воды достигается при добавлении к 1 л 99,5%-ного этилового спирта 27,5 г диэтилфталата и 7 г металлического натрия. Смесь кипятят в течение 1 ч, затем перегоняют и получают спирт, содержащий 99,95% C2H5OH.
Определение концентрации перекиси водорода
В коническую колбу с 10 мл перекиси водорода прибавляют 5 мл 10%-ного раствора серной кислоты и 1 г йодистого калия. Колбу закрывают пробкой, хорошо перемешивают и через 30 мин выделившийся йод титруют 0,1 н. раствором гипосульфита в присутствии 1%-ного раствора крахмала. 1 мл 0,1 н. раствора гипосульфита соответствует 1,701 мг перекиси водорода.
Очистка перекиси водорода от примесей серной кислоты
30%-ный раствор пергидроля смешивают с прокипяченной дистиллированной водой в соотношении 1 : 8,5. К раствору прибавляют до появления отчетливой синей окраски 0,1%-ный раствор бромфенолового синего и при взбалтывании 0,1 н. раствор едкого бария до перехода окраски раствора в пурпуровый цвет. Склянку с раствором закрывают пробкой и оставляют в темноте на 1 сутки. После отстаивания раствор сливают с осадка выпавшего сернокислого бария в сухую чистую склянку. Раствор хранят в темноте.
Очистка этилового эфира от перекисей
1 л эфира встряхивают в делительной воронке со смесью 10 мл 40%-ного раствора едкой щелочи (KOH или NaOH) и 100 мл 4%-ного раствора перманганата калия. После отстаивания нижний водный слой, окрашенный в зеленый цвет, сливают, а эфир снова встряхивают со свежей порцией щелочного раствора перманганата калия до тех пор, пока водный слой не перестанет окрашиваться в зеленый цвет. После этого эфир промывают дистиллированной водой до полного удаления щелочи (реакция на фенолфталеин).
Полноту удаления перекисей проверяют следующим образом: 20 мл эфира встряхивают с 5 мл смеси, состоящей из равных объемов 60%-ного раствора йодистого калия и 1%-ного спиртового раствора фенолфталеина. Чистый эфир не должен окрашиваться в красный цвет.
Проверка термометров
Правильность показаний термометров проверяют, пользуясь набором паспортизованных нормальных термометров. Этот способ является наиболее простым.
При проверке показаний термометр помещают рядом с нормальным термометром в одинаковые условия: в лед — проверка при 0° С и в пары кипящей дистиллированной воды — проверка при 100° С. Если необходимо проверить термометр при промежуточных температурах, то оба термометра помещают в вазелиновое масло или другое вещество.
Источник