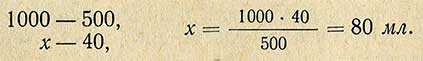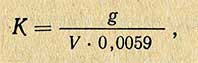Приготовление титрованного раствора NaOH
Грамм-эквивалент NaOH равен 40 г, следовательно, для приготовления 1 л 1 н. раствора требуется 40 г этого реактива. В 1 л 0,5 н. раствора соответственно должно содержаться 20 г, 0,1 н. — 4 г и т.д. Для приготовления раствора используют химически чистый реактив NaOH, растворяя его в дистиллированной воде в объеме, равном массе (весу) реактива, получая при этом насыщенный раствор NaOH.
Приготовленный раствор оставляют в склянке с резиновой пробкой на 2-3 недели для осаждения примеси карбоната натрия. После этого проверяют концентрацию полученного раствора путем титрования пробы определенного объема в присутствии индикатора метилового оранжевого. На основании полученных данных устанавливают необходимое количество насыщенного раствора NaOH для приготовления титрованного раствора.
Пример расчета. Требуется приготовить 10 л 0,1 н. раствора NaOH, для этого необходимо 10 X 4 = 40 г NaOH. Согласно проверке концентрации насыщенного раствора установлено, что в 1 л содержится 500 г NaOH. Следовательно, необходимые 40 г NaOH содержатся в следующем объеме (мл) насыщенного раствора:
Для приготовления 0,1 н. раствора необходимо взять 80 мл насыщенного раствора и довести дистиллированной водой (освобожденной от CO2 кипячением) до 10 л. Насыщенный раствор очень осторожно сливают с осадка сифоном.
Титрованный раствор щелочи хранят в склянке с пробкой, снабженной хлоркальциевой трубкой с натронной известью, для защиты от углекислого газа воздуха. Титр раствора щелочи устанавливают по янтарной кислоте или по титрованному раствору соляной кислоты.
Для установления титра 0,1 н. раствора NaOH по янтарной кислоте берут с точностью до 0,0001 г 3-4 навески химически чистой высушенной до постоянной массы (веса) кислоты по 0,20-0,25 г.
Навеску янтарной кислоты переносят в коническую колбу емкостью 250 мл и растворяют в 25-50 мл дистиллированной воды. Прибавляют к этому раствору 3-4 капли индикатора фенолфталеина и титруют раствором едкого натра до неисчезающего в течение 50-60 сек розового окрашивания. Коэффициент поправки К для титрованного раствора NaOH рассчитывают по следующей формуле:
где g — навеска янтарной кислоты, г; V — объем едкого натра, израсходованного на титрование, мл; 0,0059 — количество янтарной кислоты, соответствующее 1 мл точно 0,1 н. раствора NaCl.
Источник
Реактивы и техника приготовления растворов
Растворы щелочей. Едкие щелочи и их растворы активно поглощают влагу и углекислоту из воздуха, поэтому приготовление из них растворов точного титра затруднено. Лучше всего такие растворы изготовлять из фиксаналов. Для этого берут пробирку с фиксаналом требуемой нормальности и мерную колбу на 1 л. В колбу вставляют стеклянную воронку с вложенным в нее стеклянным бойком, острый конец которого обращен вверх.
Когда боек будет правильно уложен в воронке, ампуле с фиксаналом дают свободно падать, чтобы тонкое дно ампулы разбилось при ударе об острый конец бойка. После этого пробивают боковое углубление ампулы и дают содержимому вытечь. Затем, не меняя положения ампулы, ее тщательно промывают хорошо прокипяченной дистиллированной водой, остуженной до температуры 35- 40°С и взятой в таком количестве, чтобы по охлаждении раствора до 20°С надо было бы добавить до метки лишь несколько капель. Титрованный раствор щелочи следует хранить в таких условиях, которые исключают возможность его соприкосновения с воздухом.
Если же фиксанала нет, титрованные растворы приготовляют из препаратов едкого натра (или едкого кали). Молекулярная масса NaOH равна 40,01. Это число одновременно является и его грамм-эквивалентом.
Чтобы приготовить 1 л 1 и. раствора NaOH, нужно взять 40 г химически чистого едкого натра, а для приготовления 1 л0,1н. раствора — в десять раз меньше, т. е. 4 г.
Для удобства расчета требуемого количества исходных веществ на приготовление 1 л титрованных растворов щелочей разной нормальности рекомендуем пользоваться данными, приведенными в таблице 31.
Таблица 31
Исходные химические вещества, г
Молекулярная масса
Грамм-эквивалент
Нормальность раствора
Вещества для
установки
титров
1
0,5
0,2
0,1
0,05
0,02
0,01
NaOH
40,01
40,01
40,01
20,0
8,0
4,0
2,0
0,8
0,4
Янтарная плп щавелевая кислота
КОН
56,10
56,10
56,10
28,05
11,20
5,60
2,80
1,12
0,56
То же
Чтобы приготовить 1 л 0,1 н. раствора едкого натра, отвешивают немного больше 4 г (4,3-4,5 г) препарата и растворяют в небольшом объеме дистиллированной воды (около 7 мл).
После отстаивания раствор осторожно сливают (без осадка) в литровую мерную колбу и доводят дистиллированной свежепрокипяченной водой до метки.
Приготовленный раствор хорошо перемешивают и помещают в бутыль, защищенную от попадания углекислоты. После этого устанавливают титр, т. е. точную концентрацию раствора.
Титр можно устанавливать по щавелевой или янтарной кислоте. Щавелевая кислота (СгН204-2Н20) двухосновная, и, следовательно, ее грамм эквивалент будет равен половине молекулярной. Если молекулярная масса щавелевой кислоты равна 126,05 г, то ее грамм-эквивалент будет 126,05 : 2=63,025 г.
Имеющуюся щавелевую кислоту следует один-два раза перекристаллизовать и только после этого применять для установки титра.
Перекристаллизацию проводят следующим образом: берут произвольное количество вещества, предназначенное для перекристаллизации, растворяют нагреванием, стараясь получить возможно большую концентрацию раствора или насыщенный раствор. При необходимости этот раствор фильтруют через воронку для горячего фильтрования. Фильтрат собирают в колбу Эрленмейера, фарфоровую чашку или стакан.
В зависимости от характера кристаллизации вещества насыщенный в горячем состоянии раствор охлаждают. Для быстрого охлаждения раствора при перекристаллизации кристаллизатор помещают в холодную воду, снег или лед. При медленном охлаждении раствор оставляют стоять при температуре окружающего воздуха.
Если выпали очень мелкие кристаллы, их снова растворяют, нагревая; сосуд, в котором осуществлялось растворение, сразу же обертывают в несколько слоев полотенцем, накрывают часовым стеклом и оставляют стоять в полном покое в течение 12-15 ч.
Затем кристаллы отделяют от маточного раствора, фильтруя под вакуумом (воронка Бюхнера), тщательно отжимают, промывают и подсушивают.
Приготавливая 0,1 н. раствор NaOH, необходимо иметь раствор щавелевой кислоты такой же нормальности, для этого на 1 л раствора ее нужно взять 63,025 : 10=6,3025 г. Но для установки титра такого количества раствора щавелевой кислоты много; достаточно приготовить 100 мл. Для этого на аналитических весах отвешивают около 0,63 г перекристаллизованной щавелевой кислоты с точностью до четвертого десятичного знака, например 0,6223 г. Взятую навеску щавелевой кислоты растворяют в мерной колбе (на 100 мл). Зная массу взятого вещества и объем раствора, легко вычислить его точную концентрацию, которая в данном случае равна не 0,1 н., а несколько меньше.
Из приготовленного раствора берут пипеткой 20 мл, добавляют несколько капель фенолфталеина и титруют приготовленным раствором щелочи до появления слабого розового окрашивания.
Пусть на титрование пошло 22,05 мл щелочи. Как же определить ее титр и нормальность?
Щавелевой кислоты было взято 0,6223 г вместо теоретически рассчитанного количества 0,6303 г. Следовательно, нормальность ее будет равна не точно 0,1
Чтобы вычислить нормальность щелочи, воспользуемся соотношением VN=ViNt, т. е. произведение объема на нормальность известного раствора равно произведению объема на нормальность для неизвестного раствора. Получаем: 20-0,09873 =22,05-а:, откуда
Чтобы вычислить титр или содержание NaOH в 1 мл раствора, следует нормальность умножить на грамм-эквивалент щелочи и полученное произведение разделить на 1000. Тогда титр щелочи будет
Но этот титр не соответствует 0,1 н. раствору NaOH. Для этого прибегают к коэффициенту к, т. е. отношению практического титра к теоретическому. В данном случае он будет равен
При использовании для установки титра янтарной кислоты раствор ее приготовляют в том же порядке, что и щавелевой, исходя из следующего расчета: молекулярная масса янтарной кислоты (С4Н604) равна 118,05 г, но так как она двухосновная, то ее грамм-эквивалент 59,02 г.
Чтобы приготовить 1 л децинормального раствора янтарной кислоты, ее нужно взять в количестве 59,02 : 10 = =5,902, а для 100 мл раствора -0,59 г.
Установка титра 0,1 н. раствора NaOH весовым методом. Для установки титра 0,1 н. раствора NaOH берем навеску янтарной кислоты с точностью до 0,0001 г (например, 0,1827 г). Навеску растворяем в дистиллированной воде (около 100 мл), затем добавляем 3-5 капель фенолфталеина и титруем щелочью (NaOH). Предположим, что на титрование пошло 28 мл NaOH. Вычисление титра NaOH и поправку к нему проводим следующим образом: так как грамм-эквивалент NaOH, равный 40,01 г, соответствует грамм-эквиваленту янтарной кислоты, равному 59,02 г, то, составляя пропорцию, узнаем, какому количеству NaOH соответствует содержащееся в навеске количество янтарной кислоты: 40,01-59,02
Вычисляем титр NaOH, т. е. содержание NaOH в 1 мл раствора. Оно равно: 0,1238 : 28=0,00442. Поправка к титру NaOH равна отношению титра практического к теоретическому
Проверка нормальности раствора щелочи по титрованному раствору кислоты. В три конические колбочки отмеряют бюреткой по 20-25 мл титрованного раствора кислоты (НС1 или H2S04) и титруют раствором NaOH до изменения окраски метилоранжа.
Допустим, что на титрование трех проб по 20 мл 0,1015 н. раствора НС1 затрачено в среднем 19,50 мл раствора NaOH. Нормальность щелочи будет
Растворы кислот. В большинстве случаев в лаборатории приходится иметь дело с серной, соляной и азотной кислотами. Они находятся в виде концентрированных растворов, процентное содержание которых узнаем по плотности.
При аналитических работах используем химически чистые кислоты. Чтобы приготовить раствор той или иной кислоты, количество концентрированных кислот обычно берем по объему, вычисленному по плотности.
Например, нужно приготовить 0,1 н. раствор H2S04. Это значит, что в 1 л раствора должно содержаться
Сколько же по объему нужно взять H2S04 с плотностью 1,84, чтобы, разбавив ее до 1 л, получить 0,1 н. раствор?
Кислота с плотностью 1,84 содержит 95,6% H2S04. Следовательно, на 1 л раствора ее нужно взять в граммах:
Выражая массу в объемных единицах, получим
Отмерив из бюретки точно 2,8 мл кислоты, разбавляем ее до 1 л в мерной колбе, затем, титруя щелочью, проверяем нормальность.
Например, при титровании установлено, что 1 мл 0,1 н. раствора H2S04 содержит не 0,0049 г H2S04, а 0,0051 г. Для вычисления количества воды, которое нужно добавить к 1 л кислоты, составляем пропорцию:
Следовательно, в этот раствор нужно добавить 41 мл воды. Но учитывая, что от исходного раствора было взято на титрование 20 мл, что составляет 0,02, то воды нужно брать меньше, т. е. 41-(41-0,02) =41-0,8 =40,2 мл. Это количество воды и добавляем из бюретки в колбу с раствором.
Приведенная выше работа при выполнении довольно кропотлива, поэтому можно готовить приблизительно точные растворы, вводя поправочный коэффициент, который применяют в работе при каждом титровании. При этом израсходованное число миллилитров раствора умножаем на поправочный коэффициент.
Поправочный коэффициент вычисляем по формуле
где V — объем испытуемого раствора, взятый для титрования;
kt — поправочный коэффициент раствора щелочи известной нормальности, по которому устанавливают титр вновь приготовленного раствора кислоты;
Ух— объем раствора щелочи известной нормальности, пошедший на титрование испытуемой кислоты.
Источник
Как приготовить одномолярный раствор гидроксида натрия
§7.7 Концентрация раствора.
На практике часто приходится иметь дело с растворами, имеющими строго заданное содержание в них растворенного вещества . Приведем несколько примеров.
Во-первых, это приготовление различных лекарственных растворов. Если в аптеке случайно произойдет ошибка с количеством лекарства в его растворе, то последствия могут быть самыми плачевными.
Во-вторых, многие химические реакции проводят в растворах. И здесь ошибки могут приводить к печальным результатам. Например, если фотограф ошибется при растворении проявителя, то фотографии либо не проявятся, либо будут испорчены. Другой пример: если залить в аккумулятор раствор, в котором содержание серной кислоты будет меньше или больше требуемого, то аккумулятор либо не будет работать, либо выйдет из строя.
Еще один пример из лабораторной практики. Для получения бромистого калия (KBr) взяли два раствора: HBr и KOH. Из-за ошибки при приготовлении растворов гидроксид калия KOH добавили в воду в гораздо большем количестве, чем это требовалось для реакции обмена:
H Br + K OH = K Br + H 2 O
В результате полученный водный раствор KBr оказался безнадежно испорченным примесью непрореагировавшего, очень едкого гидроксида калия KOH.
Во всех перечисленных случаях было не учтено или нарушено заданное содержание вещества в растворе. Давайте разберемся в том, как правильно выражать это содержание и как правильно готовить раствор, если содержание вещества в растворе задано.
Один из способов выражения количества вещества в растворе – задание МАССОВОЙ ДОЛИ РАСТВОРЕННОГО ВЕЩЕСТВА .
Массовая доля растворенного вещества – это отношение массы растворенного вещества m 1 к общей массе раствора m, выраженное в процентах.
Пример 1. Для лечения гипертонической болезни (повышенное давление) применяют 25%-ный раствор сульфата магния MgSO 4 . Это означает, что в 100 г такого раствора содержится 25 г MgSO 4 . Здесь выделено слово “раствора”. Действительно, если мы взвесим 25 г сульфата магния и просто растворим в 100 г воды, то нужного нам раствора не получим.
Как же приготовить 25%-ный раствор? Надо взвесить на весах 25 г безводного сульфата магния и отмерить мензуркой 75 мл воды (либо взвесить на весах 75 г воды, что одно и то же). Затем сульфат магния надо высыпать в воду и перемешать до полного растворения. Получится 100 г раствора (25 г + 75 г = 100 г), в котором массовая доля сульфата магния составляет точно 25 %.
** Если для взвешивания 25 г MgSO 4 не найдется безводной соли, а в наличии окажется только более распространенный кристаллогидрат MgSO 4 . 7H 2 O, то необходимо взять больше соли. Предварительно следует рассчитать, в каком количестве MgSO 4 . 7H 2 O содержится 25 г MgSO 4 и взвесить именно это рассчитанное количество MgSO 4 ·7H 2 O. Соответственно, на приготовление такого раствора пойдет меньше воды, потому что часть ее уже имеется в кристаллогидрате.
Пример 2. Для заливки в новый автомобильный аккумулятор нужен 36%-ный раствор серной кислоты. Это означает, что в 100 г такого раствора содержится 36 г серной кислоты и 64 г воды (100 г — 36 г = 64 г.). Массовая доля серной кислоты в таком растворе составляет 36%.
Разумеется, 100 г раствора – слишком маленькое количество для автомобильного аккумулятора, поэтому приготовим 10 кг раствора. Для этого увеличим все цифры в 100 раз. Итак, нам потребуется взвесить на весах (36 г х 100) = 3600 г или 3,6 кг крепкой (безводной) серной кислоты и отмерить (64 г х 100) = 6400 г или 6,4 л дистиллированной воды.
Осторожно смешаем серную кислоту с водой (происходит сильный разогрев). Получим 10 кг 36%-ного раствора серной кислоты, который после охлаждения можно заливать в аккумулятор.
** Водитель, который не очень усердно изучал в школе химию, может легко ошибиться, взяв вместо 3,6 кг серной кислоты 3,6 л серной кислоты. В этом случае аккумулятор будет испорчен, потому что количество H 2 SO 4 в растворе окажется намного больше требуемого.
Дело в том, что серная кислота – довольно «тяжелая» жидкость, ее плотность 1,84 кг/л. Можно подсчитать, какой объем займет серная кислота массой 3,6 кг:
1 л H2 SO 4 весит 1,84 кг (плотность серной кислоты)
х л H2 SO 4 весят 3,6 кг
Отсюда х = 1 л . 3,6 кг/1,84 кг = 1,956 л – такой объем (меньше двух литров!) занимает концентрированная кислота весом 3,6 кг.
Массовую долю растворенного вещества называют также ПРОЦЕНТНОЙ КОНЦЕНТРАЦИЕЙ раствора.
Концентрация – это относительное количество растворенного вещества в растворе.
Помимо процентной концентрации, часто удобно пользоваться МОЛЯРНОЙ КОНЦЕНТРАЦИЕЙ .
Молярная концентрация С – это отношение количества растворенного вещества v (в молях) к объему раствора V в литрах.
Единица молярной концентрации – моль/л. Зная число молей вещества в 1 л раствора, легко отмерить нужное количество молей для реакции с помощью подходящей мерной посуды.
В качестве примера рассмотрим получение нерастворимого в воде хлорида серебра (AgCl) с помощью реакции обмена:
AgNO 3 + NaCl = Ag Cl (осадок) + Na NO 3
Кстати, не нужно запоминать, какие соли растворимы, а какие нерастворимы в воде. Для этого существует таблица растворимости (теперь она есть и в меню левого окна).
Допустим, в лаборатории имеется раствор AgNO 3 , концентрация которого 1 моль/л. Это означает, что в 1 л такого раствора содержится 1 моль нитрата серебра.
По уравнению реакции на 1 моль AgNO 3 нужен 1 моль NaCl. Следовательно, если мы смешаем одинаковые объемы растворов AgNO 3 и NaCl одинаковой концентрации 1 моль/л, то реакция пройдет до конца и в реакционной колбе окажется только раствор нитрата натрия (NaNO 3 ) в воде, а на дно сосуда выпадет осадок хлорида серебра AgCl. При этом исходных соединений в сосуде не останется.
Но как приготовить для реакции нужный раствор NaCl ? Для этого существуют специальные мерные колбы (рис. 7-4).
Рис. 7-4. Последовательность приготовления молярного раствора хлорида натрия (1моль/л NaCl): а) берут мерную колбу емкостью 1 л; б) помещают в колбу навеску кристаллического NaCl. в) в колбу добавляют немного дистиллированной воды, растворяют кристаллы и доливают раствор водой до метки 1 л, после чего тщательно перемешивают.
Мерная колба представляет собой сосуд с тонкой шейкой, на которой по стеклу нанесена кольцеобразная метка. Если заполнить мерную колбу жидкостью до метки, то ее объем составит ровно 1 л. Возьмем такую колбу и приступим к приготовлению нужного нам раствора NaCl.
Молекулярный вес NaCl составляет (23 + 35,5) = 58,5. Следовательно, молярная масса NaCl (масса 1 моль) равна 58,5 г. Взвесим это количество NaCl на весах и поместим кристаллы в мерную колбу. Затем добавим немного воды и растворим кристаллы, покачивая колбу. Когда вся соль растворится, дольем раствор водой до метки. Мерные колбы делают таким образом, что объем раствора достигает точно 1 л, когда водный мениск (уровень воды, слегка изогнутый силами поверхностного натяжения) касается метки своей нижней частью. После этого раствор аккуратно перемешаем.
** Молярную концентрацию (или МОЛЯРНОСТЬ растворов) принято обозначать буквой М. Например, раствор концентрации 1 М содержит 1 моль вещества на литр раствора. Такой раствор называют МОЛЯРНЫМ . Раствор концентрации 0,1 М содержит 0,1 моль вещества на литр раствора и называется ДЕЦИМОЛЯРНЫМ . Растворы концентрации 0,01 М (или 0,01 моль на литр) иногда называют САНТИМОЛЯРНЫМИ .
Итак, мы приготовили раствор NaCl , концентрация которого составляет 1 моль/л, то есть одномолярный или просто молярный раствор.
Молярные концентрации в общем виде иногда обозначают следующим образом:
C NaCl = 1 моль/л
При смешивании любых равных объемов молярных растворов AgNO 3 и NaCl всегда будет получаться только раствор NaNO 3 в воде и осадок AgCl , не содержащие примеси ни одного из исходных реагентов. Отфильтровав осадок и промыв его водой, мы получим чистую соль AgCl (она в воде практически не растворяется). Упарив отфильтрованный раствор, мы получим только чистый нитрат натрия NaNO 3 . Это не удивительно, потому что смешивая равные объемы растворов, мы берем одинаковое количество молей (или частей моля) реагирующих веществ. В них содержится одинаковое количество молекул AgNO 3 и NaCl , которые реагируют между собой без остатка.
На фотографии слева показан опыт, который мы обсуждаем. Видно, как при смешивании растворов исходных солей выпадает белый осадок AgCl.
Если бы мы взяли не молярные, а, например, 10%-ные растворы AgNO 3 и NaCl (одинаковые объемы), то в них бы содержалось разное число молекул этих веществ и одна из этих солей не израсходовалась бы полностью и осталась в растворе. Какая же из двух солей оказалась бы в избытке? Та, число молей которой больше. Это будет NaCl – соль с меньшим молекулярным весом, поскольку в одинаковой массе солей число более легких молекул (и молей) NaCl оказывается б о льшим.
Каждый способ выражения концентрации раствора удобен в зависимости от цели, которую преследует химик или технолог. Процентные концентрации более удобны в технике, медицине, экологии. Молярные концентрации чаще встречаются в лабораторной практике.
Источник