- Как приготовить раствор грисса
- Реактив Грисса – что это?
- Способы получения реактива Грисса
- Приготовление реактива Грисса в лабораторных условиях
- Реактив Грисса приготовленный по ТУ 6-09-3569-86
- Порошок для приготовления реактива Грисса по ГОСТ 4517-87
- Способ определения нитритов с применением реактива Грисса
- Меры безопасности при работе с опасными веществами
- Реактив Грисса для определения нитритов и нитрит-ионов
- Метод Грисса
- Приготовление реактива Грисса из порошка или жидких компонентов
Как приготовить раствор грисса
Ответов в этой теме: 8
 [ Ответ на тему ]
[ Ответ на тему ] 
 |
| Автор | Тема: Реактив Грисса и ошибки в МВИ |
| Syrop4ik Пользователь Ранг: 3
|  31.01.2020 // 4:41:04 Редактировано 1 раз(а) 31.01.2020 // 4:41:04 Редактировано 1 раз(а) Есть проблема, связанная с приготовлением реактива Грисса. Закупаем готовый смешанный реактив Грисса (чда, ТУ 6-09-3569-86) Работали на науку. Всю жизнь готовили Грисса простым растворением в горячей воде (10 г на 100 г воды), с последующим фильтрованием. Определение нитритов и нитратов (после восстановления на кадмиевом редукторе) проходило идеально. С некоторых пор аккредитовались и начали работать по РД’шкам. В этих РД прописано приготовление реактива Грисса из сухого смешанного реактива растворением его в 12% уксусной кислоте. И вот тут у нас, что называется, нашла коса на камень. Растворяем в воде — опять все идеально. Градуировки получаются стабильные и очень сексуальные. Залез в ТУ 6-09-3569-86. Появились подозрения, что составители этих РД тупо скопировали методику приготовления раствора реактива из какой-то еще более древней методики, не удосужившись проверить ее собственными руками. Имел беседу на этот счет с «экспертами», которые приехали подтверждать компетентность нашей лаборатории. Они заявляют, что «быть такого не может, делайте как написано, изменение прописи приготовления реактива это отход от методики измерений и вообще ата-та»! Что нам делать и как нам быть? Спасибо, что прочитали до конца. |
| ANCHEM.RU Администрация Ранг: 246 |  |
| OldBrave VIP Member Ранг: 1163 |  31.01.2020 // 18:26:04 Редактировано 1 раз(а) 31.01.2020 // 18:26:04 Редактировано 1 раз(а)
Вам нужны шашечки или ехать? |
| darkkiss Пользователь Ранг: 124 |  01.02.2020 // 14:12:35 01.02.2020 // 14:12:35 Валидацию методики сделайте с прописанными изменениями в приготовлении раствора. |
| lrjourney11 Пользователь Ранг: 119 |  02.02.2020 // 10:51:08 02.02.2020 // 10:51:08 Валидацию методики сделайте с прописанными изменениями в приготовлении раствора. Считаю надо разработчикам НД шек писать об ошибках, получить от них ответ, а уже потом валидировать с изменением. |
| Syrop4ik Пользователь Ранг: 3 |  03.02.2020 // 5:05:44 03.02.2020 // 5:05:44
А что, так можно было? Вы сами так делали? Поделитесь опытом? Так ведь «довалидироваться» можно до того, что методика изменится до неузнаваемости. А метрологически аттестовывать измененную методу кто будет? И какой тогда смысл в этих официальных методиках, если все «валидируют» как бог на душу положит. Не понравилась методика приготовления реактива — а «провалидирую-ка я ее», так что ли? Я сейчас методику определения нитритов из руководства Алекина «провалидирую» и буду по ней работать, а мне потом по башке настучат. Я собственно и спрашиваю: Неужели никто не сталкивался с таким? Понимаете, мне не нужна «теория» — сделайте то, сделайте это, исходя из абстрактных соображений. Мне нужен ответ практика — «была у нас похожая история, сделали вот эдак». Вы уж извините, вам наверное кажется, что я задаю архиглупейшие вопросы, но мы никогда с таким дела не имели. Работали как нормальные люди. Стабильность градуировки проверили и хватит. У нас тут метрологов и статистиков нет. Но вот по какой-то неведомой причине руководсто решило, что быть нам аккредитоваными. И тут все заверте. Пока склоняюсь к двум вариантам — «написать разработчикам методики» и «обосновать отделу закупок, почему вместо одного смешанного реактива Грисса нам нужно закупать два раздельных — нафтиламин и сульфанилку». И второй вариант похож на «дохлый номер» больше первого. Спасибо за внимание. |
| kot Пользователь Ранг: 1796 |  03.02.2020 // 9:01:11 03.02.2020 // 9:01:11
Источник Реактив Грисса – что это?Многие знают о роли индикаторов в определении наличия вещества или кислотности среды. Они используются как определители конца реакции, меняющие цвет раствора. Реактив Грисса выявляет нитриты, подробнее узнать больше можно тут. Его готовят в лабораторных условиях, смешивая два раствора, или получают промышленным способом. Способы получения реактива Грисса
Приготовление реактива Грисса в лабораторных условияхПолучить смесь органических веществ в нужной пропорции можно, используя свежую смесь двух растворов.
Растворы можно долго хранить в бутылях из темного стекла с притертыми пробками. Для получения реактива Грисса составы смешивают в равных объемах. Смесь используется в день приготовления. Есть и другие способы получения нужных реагентов, все они основаны на получении диазосоединения, меняющего окраску раствора в присутствии 1-нафтиламина. При работе нужно соблюдать меры предосторожности – работать в резиновом фартуке, очках, респираторе. Руки защитить резиновыми перчатками. Реактив Грисса приготовленный по ТУ 6-09-3569-86Промышленный выпуск реактива Грисса позволил получить смесь компонентов в нужной пропорции в сухом виде. Согласно ТУ 6-09-3569-86 изготавливают растворимую в воде смесь:
В инструкции по применению написано, рабочий раствор концентрацией 10 % готовят, разбавляя навеску дистиллированной водой. Сухой реактив содержит нужное количество кислоты для создания среды. Хранят состав в темной упаковке с притертой пробкой. Если порошок приобрел розоватый цвет, реактив испорчен. Порошок для приготовления реактива Грисса по ГОСТ 4517-87Согласно методике, реактив поставляется в сухом виде и представляет смесь альфа-нафтиламина, уксусной и сульфоновой кислоты в виде кристаллов. Состав готовят, растворяя порошок в 12 % растворе уксусной кислоты. Используют раствор в концентрации 10 %. Реактив Гесса выпускается также в компонентном составе. Растворителем служит 30 % уксусная кислота:
Используют растворы в соотношении 1:1 в этот же день. Жидкость прозрачная. Появление розового цвета говорит об испорченных реактивах или недостаточной чистоте посуды и бидистиллированной воды. Способ определения нитритов с применением реактива ГриссаЦелью анализа является количественное определение нитритов, так как этот показатель нормируется в продуктах, почве и питьевой воде. Пробу готовят, используя коагуляцию, фильтрование и другие методы. Определение возможно в прозрачном растворе с нейтральной средой. При добавлении реактива Грисса проба окрашивается в розовый цвет, в течение 40 минут интенсивность окраски усиливается. Количественный анализ ведется на фотометре, сравнением цветности стандартных растворов и пробы при длине волны 520 нм. Чувствительность высока. Содержащий микроны нитритов раствор окрашивается. Этим методом можно вести количественное определение нитритов в диапазоне 0,1-15 мкг/л. Меры безопасности при работе с опасными веществамиРабота с агрессивными жидкостями 2-3 класса опасности требует специальной подготовки лаборанта. Он должен владеть приемами работы с кислотами, иметь не менее 6 месяцев опыта разведения растворов. Лучше выполнять подготовку реактивов в вытяжном шкафу – смеси имеют очень неприятный специфический запах. Попадая на кожу, состав вызывает химический ожог. Перевозить реактив можно в любом транспорте с условием, что тара хорошо защищает реагент от высыпания и проливания. Источник Реактив Грисса для определения нитритов и нитрит-ионовРеактивом Грисса называют раствор сульфаниловой кислоты и альфа-нафтиламина Помимо указанного выше применения в фотометрии, этот хим реактив используется в аналитической химии, в сельском хозяйстве, для определения качества воды, в том числе грунтовой, питьевой и бытовой. Определение азотосодержащих соединений в воде и почве имеет огромное хозяйственное значение, так как азот важен для жизнедеятельности живых организмов, особенно растений. Недостаток азота в воде или почве может вызвать прекращение роста растений, а его переизбыток приводит к ухудшению качества воды и условий для микроорганизмов и флоры. Российский ГОСТ нормирует содержание нитритов в почвах и природных водах. Чувствительность определения количества нитритов методом Грисса составляет 0,002 мг/л. Диапазон измерений — от 0,1 до 15 мкг. Метод Грисса
Для определения нитритов в органических объектах по методу Грисса исследуют их водные вытяжки. Сначала биологический материал настаивают в воде, потом раствор фильтруют, удаляя взвешенные частицы. В случае необходимости применяют коагулянт, добиваясь, чтобы вытяжка стала прозрачной и бесцветной. В конце раствор пропускают через мембранный фильтр. Полученную вытяжку доводят до нейтральной реакции и подвергают воздействию реактива Грисса. Если в вытяжке присутствуют нитриты, то образуется азокраситель красного цвета. Чем окраска раствора интенсивнее, тем больше в нем нитритов. Количественные характеристики определяются с помощью фотометра или спектрофотометра на длине волны 520 нм по отношению к смеси дистиллированной воды и реактива Грисса. Содержание нитритов в микрограммах вычисляют по калибровочному графику или по шкале стандартных растворов. Приготовление реактива Грисса из порошка или жидких компонентовРеактив Грисса выпускается в виде растворимого в воде порошка белого, серого или розоватого цвета. В герметичной таре, без доступа света соединение в сухой форме может храниться до 3-х лет. Для аналитических работ применяется 10-процентный раствор вещества в 12%-ной уксусной кислоте. Приготовленный раствор не должен иметь окраски и может храниться в холодильнике в герметично укупоренной посуде из темного стекла до двух суток. Также Реактив Грисса может поставляться в виде двух составляющих: альфа-нафтиламина и сульфаниловой кислоты. Для приготовления собственно реактива отдельно готовят в 30%-ном растворе уксусной кислоты: Потом оба раствора смешивают в равных пропорциях. Готовое соединение должно быть бесцветным. Приготовленный этим способом реактив следует использовать в тот же день. Отдельные составные части хранятся дольше и их можно готовить заранее. Раствор альфа-нафтиламина нужно хранить в герметично закрытой склянке из темного стекла. Приготовление раствора Грисса требует от лаборанта умения работы с опасными Реактив Грисса относится к веществам 2-3 класса опасности. Соединение токсично, при попадании на кожу и слизистые вызывает химический ожог. Готовить реактив, а также проводить с ним анализы разрешается в проветриваемом помещении с общей приточно-вытяжной и местной вентиляцией, с применением защитных средств: резиновых перчаток, спецодежды, противогазов или защитных очков и респираторов. Помимо реактива Грисса в порошке, в химическом магазине «ПраймКемикалсГрупп» можно купить необходимые принадлежности для работы с ним: мембранные фильтры, посуду из темного стекла, средства защиты. Источник |
 Нитритные радикалы проявляет себя изменением цвета среды в момент синтеза нового вещества с изменением валентности азота. Реактив Грисса представляет набор активных компонентов, которые создадут сложную молекулу, если в испытуемом растворе есть HNO2. Смесь химических веществ виннокислого 1-нафтиламина, винной и сульфаниловой кислот в растворе окрашивается в присутствии азотистой кислоты. Чем интенсивнее будет цвет раствора, тем большая концентрация органических соединений нитритов в пробе. Определения количества вещества по цветности раствора происходит фотометрическим способом.
Нитритные радикалы проявляет себя изменением цвета среды в момент синтеза нового вещества с изменением валентности азота. Реактив Грисса представляет набор активных компонентов, которые создадут сложную молекулу, если в испытуемом растворе есть HNO2. Смесь химических веществ виннокислого 1-нафтиламина, винной и сульфаниловой кислот в растворе окрашивается в присутствии азотистой кислоты. Чем интенсивнее будет цвет раствора, тем большая концентрация органических соединений нитритов в пробе. Определения количества вещества по цветности раствора происходит фотометрическим способом.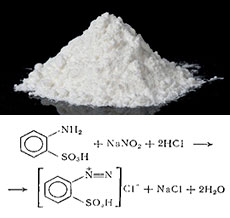 в разбавленной уксусной кислоте. Названо соединение в честь немецкого химика-органика, предложившего его в 1858-м году для фотометрического определения нитритов, азотистой кислоты, некоторых типов органических веществ, которые выделяют азотистую кислоту при нагревании. Готовый реактив имеет очень маленький срок хранения, поэтому его обычно готовят непосредственно перед применением из порошка или жидких компонентов. Порошок «Реактив Грисса ЧДА» вы можете купить в нашем магазине, а как приготовить реактив, мы расскажем ниже.
в разбавленной уксусной кислоте. Названо соединение в честь немецкого химика-органика, предложившего его в 1858-м году для фотометрического определения нитритов, азотистой кислоты, некоторых типов органических веществ, которые выделяют азотистую кислоту при нагревании. Готовый реактив имеет очень маленький срок хранения, поэтому его обычно готовят непосредственно перед применением из порошка или жидких компонентов. Порошок «Реактив Грисса ЧДА» вы можете купить в нашем магазине, а как приготовить реактив, мы расскажем ниже.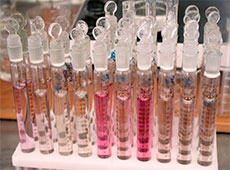 Метод Грисса основан на получении диазосоединений, которые в результате реакции с альфа-нафтиламином окрашивают раствор в красный цвет.
Метод Грисса основан на получении диазосоединений, которые в результате реакции с альфа-нафтиламином окрашивают раствор в красный цвет. веществами. По требованиям ГОСТа готовить соединение могут лаборанты с опытом работы не менее полугода.
веществами. По требованиям ГОСТа готовить соединение могут лаборанты с опытом работы не менее полугода.