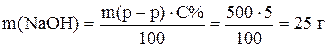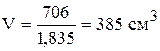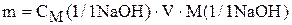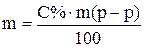- Приготовление растворов солей с определенной массовой долей растворенного вещества
- Правила техники безопасности
- ХОД УРОКА
- Этапы выполнения работы
- Взвешивание (6–7 мин)
- Домашнее задание
- Карточка учета умений
- Образцы отчета о проделанной практической работе
- Способы приготовления растворов заданной концентрации
Приготовление растворов солей
с определенной массовой долей
растворенного вещества
Практическая работа выполняется по инструкции и содержит несколько вариантов. Каждый ученик выбирает один из пяти предложенных вариантов задач. Задания, обозначенные звездочкой (*), предназначены для учащихся, успешно выполнивших предыдущие задания.
Цели. Уметь готовить растворы с определенной массовой долей растворенного вещества, используя следующие операции: взвешивание, отмеривание определенного объема жидкости, растворение; производить необходимые расчеты; знать расчетную формулу для определения массовой доли растворенного вещества, правила пользования химической посудой и реактивами.
Оборудование. Технические весы с разновесами, химический стакан, мерный цилиндр, ложечка для сыпучих веществ, стеклянная палочка, склянка под приготовленный раствор.
Реактивы. NaCl, Н3ВO3, СuSO4, NaHCO3 – все кристаллические, 30%-й раствор NaOH, дистиллированная (кипяченая) вода.
Подготовить для приготовляемых растворов склянки с этикетками, на которых формула изображена в цвете: для кислот – красным, для солей – черным, для щелочей – синим.
Правила техники безопасности
Осторожно обращайтесь с химическим оборудованием!
Пользуйтесь чистой и пригодной для работы посудой.

Запрещается пробовать вещества на вкус (а),
брать вещества руками (б),
оставлять неубранными рассыпанные
или разлитые реактивы (в),
оставлять открытыми склянки с жидкостями
и банки с сухими веществами (г);
работу проводить только над столом (д)
Предварительно учащиеся получают домашнее задание, связанное с изучением содержания предстоящей работы по инструкции, используя материал учебников 8-го класса авторов О.С.Габриеляна (§ 34) или Г.Е.Рудзитиса, Ф.Г.Фельдмана (§ 30).
ХОД УРОКА
В письменном отчете записываются название темы, цели, оборудование, реактивы (4–5 мин).
Предлагается несколько вариантов расчетных задач для приготовления растворов и пример решения задачи.
Вариант № 1
Определите массы воды и борной кислоты, необходимые для приготовления 50 г раствора с массовой долей кислоты 0,02. Где применяют данный раствор?
Вариант № 2
Какие массы гидрокарбоната натрия и воды надо взять, чтобы приготовить раствор массой 50 г с массовой долей соли 10%? Где используют данный раствор?
Вариант № 3
В 45 г воды растворено 5 г NaCl. Вычислите массовую долю растворенного вещества в растворе. Для чего необходим этот раствор в быту и лаборатории?
Вариант № 4 *
Рассчитайте массы воды и безводного сульфата меди, необходимые для приготовления 100 мл раствора, содержащего 8% соли. плотность раствора – 1,084 г/мл. Где применяют полученный раствор?
Вариант № 5 *
Какую массу воды нужно добавить к 100 мл 30%-го раствора гидроксида натрия ( 
Пример решения задачи
Вычислите массы соли и воды, которые потребуются для приготовления 50 г раствора хлорида натрия, содержащего 0,1 массовой доли соли.
Этапы выполнения работы
1. После произведенных расчетов по одному из вариантов оформите их в тетради (6–7 мин).
2. Отвесьте рассчитанное количество вещества и поместите его в стакан объемом 100 мл или колбу на 200 мл.
Помните! К соли приливают воду! Кислоту добавляют в воду при постоянном перемешивании!
Взвешивание
(6–7 мин)

Технохимические весы:
1 – стойка; 2 – стремена; 3 – коромысло;
4 – чашка; 5 – стрелка; 6 – ручка арретира
· Отрегулируйте арретиром весы.
· Взвешиваемое вещество кладите на левую чашку весов, разновесы на правую. (Для левшей – на правую чашку кладут вещество, на левую – разновесы.)
· Разновесы брать только пинцетом и при снятии с весов класть сразу в те гнезда футляра, из которых они были взяты.
· После взвешивания чашка весов должна оставаться чистой.
· По окончании работы проверьте разновесы. Весы арретировать (привести в нерабочее состояние).
Жидкости на весах не взвешивают !
3. Отмерьте мерным цилиндром рассчитанный объем жидкости и вылейте в стакан с солью или водой (1–2 мин).
4. Перемешайте стеклянной палочкой смесь до полного растворения вещества. Раствор готов!
5. В отчете опишите последовательность ваших действий. Сделайте рисунок сосуда, в котором вы приготовили раствор (10 мин). 
Пример. 0,9%-й раствор NaCl называется физиологическим. Применяется для инъекций.
6. Сделайте письменный вывод о проделанной работе (5–6 мин).
7. Приведите рабочее место в порядок (1–2 мин).
Сдайте тетради на проверку.
Домашнее задание
Задача. Определите массу воды, которую нужно добавить к 50 г раствора с массовой долей соли 5%, чтобы получить раствор с массовой долей соли 2%.
Учитель следит за выполнением работы учащимися и отмечает свои наблюдения в карточке учета умений.
Карточка учета умений
| Операции практической работы | Фамилии учащихся | |||||
|---|---|---|---|---|---|---|
| А | Б | В | Г | Я | ||
| Приготовление склянки для раствора | ||||||
| Знание правил техники безопасности | ||||||
| Взвешивание вещества | ||||||
| Работа с мерным цилиндром | ||||||
| Приготовление раствора | ||||||
| Kультура выполнения опыта | ||||||
| Оформление отчета | ||||||
Образцы отчета о проделанной
практической работе
Вариант № 1
Взвешиваю 1 г борной кислоты, помещаю его в стакан и добавляю к веществу воды до метки 50 мл. Вещество растворяется в воде. Для его лучшего растворения перемешиваю раствор стеклянной палочкой. Переливаю раствор в приготовленную склянку с этикеткой.
Раствор борной кислоты используют в медицине как дезинфицирующее средство.
В лаборатории он хранится в аптечке для промывания глаз в случае попадания в них щелочи.
Вариант № 2
Взвешиваю 5 г гидрокарбоната натрия и помещаю в химический стакан вместимостью 50 мл (или 100 мл). Добавляю воды до метки 50 мл. Вещество растворяется. для его полного растворения перемешиваю раствор стеклянной палочкой. Получила 10%-й раствор NaHCO3. Переливаю раствор в склянку с этикеткой.
Полученный раствор используют для обработки кожного покрова в случае попадания на него кислоты.
Вариант № 3
Взвешиваю на весах 5 г хлорида натрия и помещаю соль в химический стакан. Мерным цилиндром отмериваю 45 мл воды и добавляю к соли. Для лучшего растворения соли перемешиваю раствор стеклянной палочкой. Переливаю раствор в приготовленную склянку.
Раствор используют в быту для засолки огурцов и квашения капусты. В лаборатории раствор NaCl используют как реактив для проведения химическиx реакций.
Вариант № 4 *
Взвешиваю на весах 8,7 г соли CuSO4. Отмериваю мерным цилиндром 100 мл воды и переливаю в стакан с солью. Перемешиваю раствор стеклянной палочкой. Приготовленный раствор переношу в склянку с этикеткой.
Раствор используют для борьбы с вредителями сельскохозяйственных культур.
Вариант № 5 *
Добавим к выданному 30%-му раствору щелочи 266 мл воды. Получили 10%-й раствор NаОН.
Внимание! Если для приготовления растворов берут щелочь в кристаллическом виде, тогда щелочь добавляют в воду.
Раствор используют в химической лаборатории для проведения химических реакций.
Вывод. Рассчитав массу вещества и объем воды, приготовили раствор с заданной концентрацией растворенного вещества, используя операции: взвешивание, отмеривание объема жидкости, растворение. Растворы широко применяются в быту и народном хозяйстве.
Источник
Способы приготовления растворов заданной концентрации



С помощью технических или аналитических весов (в зависимости от заданной точности приготовления) отвешивают расчетное количество твердого вещества, переносят в мерную посуду, растворяют в небольшом количестве воды и доливают дистиллированную воду до отметки заданного объема (доводят до метки). Растворы можно готовить также разбавлением более концентрированных растворов.
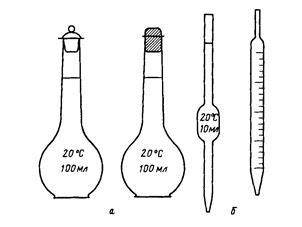
Рис. 1. Мерные колбы (а), пипетки (б)
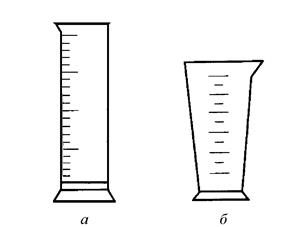
Рис. 2. Мерный цилиндр (а), мерный стакан (мензурка) (б)
Пример 1. Приготовить 0,5 дм 3 15 г/дм 3 раствора гидроксида натрия. Рассчитаем массу вещества по уравнению (1)
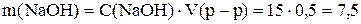
Навеску 7,5 г растворяем в мерной колбе на 500 см 3 .
Приготовление растворов с заданной массовой долей. Растворы готовят в химически стойкой посуде без градуировки объема. С помощью технических или аналитических весов отвешивают расчетное количество твердого вещества, переносят в мерную посуду и растворяют в расчетном количестве воды. Такие растворы можно готовить разбавлением концентрированных или смешением концентрированных и более разбавленных (или воды) растворов.
Пример 2. Приготовить 500 г 5% раствора гидроксида натрия. По уравнению (2) рассчитаем массу NaOH
Масса воды равна
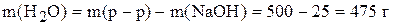
Таким образом, для приготовления раствора надо растворить 25 г твердого NaOH в 475 г воды.
Пример 3. Приготовить 3 кг 30% раствора серной кислоты из 95% и 10% раствора. Для приготовления необходимо рассчитать массы обоих растворов. Ранее для этого рекомендовали использовать правило «креста», в настоящее время с развитием вычислительной техники проще решить систему двух уравнений или воспользоваться готовой формулой. Введем обозначения x – необходимая масса 95% кислоты; y — необходимая масса 10% кислоты; m – масса конечного раствора, С%(1) – массовая доля 95% кислоты; С%(2) – массовая доля 10% кислоты; С%(к) – массовая доля приготовляемой кислоты.
Сумма масс кислоты в исходных растворах равна массе кислоты в конечном растворе, сумма масс растворов исходных кислот равна массе приготовляемой кислоты. Тогда получим систему из двух уравнений
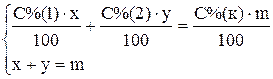
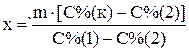
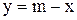
Подставив численные значения, получим:
х = 706 г; y = 2294 г.
Часто удобнее пользоваться не массой, а объемом растворов. В этом случае по справочнику определяют плотность исходных растворов и рассчитывают их объемы:
Для 95% кислоты 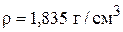
Для 10% кислоты 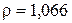
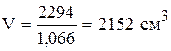
Таким образом, для приготовления 3 кг 30% раствора серной кислоты необходимо отмерить 385 см 3 95% кислоты и прибавить 2152 см 3 10% кислоты.
Если в качестве второго раствора берут чистую воду, то принимают С%(2) = 0.
Приготовление растворов с заданной молярной концентрацией или молярной концентрацией эквивалента. Растворы готовят в специальной мерной посуде: мерных колбах, мерных цилиндрах (рис. 1, 2). С помощью технических или аналитических весов отвешивают расчетное количество твердого вещества, переносят в мерную посуду, растворяют в небольшом количестве воды и доливают дистиллированную воду до отметки заданного объема (доводят до метки). Такие растворы можно готовить также разбавлением более концентрированных растворов.
Пример 4. Приготовить 250 см 3 раствора NaOH с концентрацией 0,5 н из 10% раствора, r = 1,11 г/см 3 .
Массу NaOH, необходимую для приготовления раствора рассчитаем из уравнения (3)
Такая же масса NaOH должна содержаться в пробе 10% раствора
Приравняв правые части уравнений получим
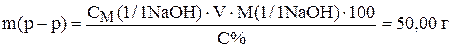
Рассчитаем объем раствора
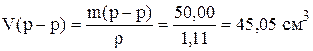
Таким образом, для приготовления раствора необходимо в мерную колбу на 250 см 3 отмерить 45,05 см 3 раствора NaOH с концентрацией 10%, довести до метки дистиллированной водой, и перемешать.
Источник