Расчеты при приготовлении водных растворов
Приблизительные растворы. При приготовлении приблизительных растворов количества веществ, которые должны быть взяты для этого, вычисляют с небольшой точностью. Атомные веса элементов для упрощения расчетов допускается брать округленными иногда до целых единиц. Так, для грубого подсчета атомный вес железа можно принять равным 56 вместо точного —55,847; для серы — 32 вместо точного 32,064 и т. д.
Вещества для приготовления приблизительных растворов взвешивают на технохимических или технических весах.
Принципиально расчеты при приготовлении растворов совершенно одинаковы для всех веществ.
Количество приготовляемого раствора выражают или в единицах массы (г, кг), или в единицах объема (мл, л), причем для каждого из этих случаев вычисление количества растворяемого вещества проводят по-разному.
Пример. Пусть требуется приготовить 1,5 кг 15%-ного раствора хлористого натрия; предварительно вычисляем требуемое количе-ство соли. Расчет проводится согласно пропорции:

т. е. если в 100 г раствора содержится 15 г соли (15%), то сколько ее потребуется для приготовления 1500 г раствора?
Расчет показывает, что нужно отвесить 225 г соли, тогда воды иужио взять 1500 — 225 = 1275 г. ¦
Если же задано получить 1,5 л того же раствора, то в этом случае по справочнику узнают его плотность, умножают последнюю на заданный объем и таким образом находят массу требуемого количества раствора. Так, плотность 15%-нoro раствора хлористого натрия при 15 0C равна 1,184 г/см3. Следовательно, 1500 мл составляет

Следовательно, количество вещества для приготовления 1,5 кг и 1,5 л раствора различно.
Расчет, приведенный выше, применим только для приготовления растворов безводных веществ. Если взята водная соль, например Na2SO4-IOH2O1 то расчет несколько видоизменяется, так как нужно принимать во внимание и кристаллизационную воду.
Пример. Пусть нужно приготовить 2 кг 10%-ного раствора Na2SO4, исходя из Na2SO4 *10H2O.
Молекулярный вес Na2SO4 равен 142,041, a Na2SO4*10H2O 322,195, или округленно 322,20.
Расчет ведут вначале па безводную соль:

Следовательно, нужно взять 200 г безводной соли. Количество десятиводной соли находят из расчета:

Воды в этом, случае нужно взять: 2000 — 453,7 =1546,3 г.
Так как раствор не всегда готовят с пересчетом на безводную соль, то на этикетке, которую обязательно следует наклеивать на сосуд с раствором, нужно указать, из какой соли приготовлен раствор, например 10%-ный раствор Na2SO4 или 25%-ный Na2SO4*10H2O.
Часто случается, что приготовленный ранее раствор нужно разбавить, т. е. уменьшить его концентрацию; растворы разбавляют или по объему, или по массе.
Пример. Нужно разбавить 20%-ный раствор сернокислого аммония так, чтобы получить 2 л 5%-иого раствора. Расчет ведем следующим путем. По справочнику узнаем, что плотность 5%-ного раствора (NH4)2SO4 равна 1,0287 г/см3. Следовательно, 2 л его должны весить 1,0287*2000 = 2057,4 г. В этом количестве должно находиться сернокислого аммония:

Теперь можно подсчитать, сколько нужно взять 20%-ного рас* твора, чтобы получить 2 л 5%-ного раствора.

Полученную массу раствора можно пересчитать на объем его. Для этого массу раствора делят на его плотность (плотность 20%-ного раствора равна 1.1149 г/см3), т. е.

Учитывая, что при отмеривании могут произойти потери, нужно взять 462 мл и довести их до 2 л, т. е. добавить к ним 2000—462 = = 1538 мл воды.
Если же разбавление проводить по массе, расчет упрощается. Но вообще разбавление проводят из расчета на объем, так как жидкости, особенно в больших количествах, легче отмерить по объему, чем взвесить.
Нужно помнить, что при всякой работе как с растворением, так и с разбавлением никогда не следует выливать сразу всю воду в сосуд. Водой ополаскивают несколько раз ту посуду, в которой проводилось взвешивание или отмеривание нужного вещества, и каждый раз добавляют эту воду в сосуд для раствора.
Когда не требуется особенной точности, при разбавлении растворов или смешивании их для получения растворов другой концентрации можно пользоваться следующим простым и быстрым способом.
Возьмем разобранный уже случай разбавления 20%-ного раствора сернокислого аммония до 5%-ного. Пишем вначале так:

где 20 — концентрация взятого раствора, 0 — вода и 5’—-требуемая концентрация. Теперь из 20 вычитаем 5 и полученное значение пишем в правом нижнем углу, вычитая же нуль из 5, пишем цифру в правом верхнем углу. Тогда схема примет такой вид:

Это значит, что нужно взять 5 объемов 20%-ного раствора и 15 объемов воды. Конечно, такой расчет не отличается точностью.
Если смешивать два раствора одного и того же вещества, то схема сохраняется та же, изменяются только числовые значения. Пусть смешением 35%-ного раствора и 15%-ного нужно приготовить 25%-ный раствор. Тогда схема примет такой вид:

т. е. нужно взять по 10 объемов обоих растворов. Эта схема дает приблизительные результаты и ею можно пользоваться только тогда, когда особой точности не требуется.Для всякого химика очень важно воспитать в себе привычку к точности в вычислениях, когда это необходимо, и пользоваться приближенными цифрами в тех случаях, когда это не повлияет на результаты работы.Когда нужна большая точность при разбавлении растворов, вычисление проводят по формулам.
Разберем несколько важнейших случаев.
Приготовление разбавленного раствора. Пусть с — количество раствора, m%—концентрация раствора, который нужно разбавить до концентрации п%. Получающееся при этом количество разбавленного раствора х вычисляют по формуле:
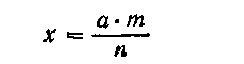
а объем воды v для разбавления раствора вычисляют по формуле:
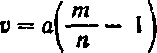
Смешивание двух растворов одного и того же вещества различной концентрации для получения раствора заданной концентрации. Пусть смешиванием а частей m%-ного раствора с х частями п%-ного раствора нужно получить /%-ный раствор, тогда:

Точные растворы. При приготовлении точных растворов вычисление количеств нужных веществ проверят уже с достаточной степенью точности. Атомные весы элементов берут по таблице, в которой приведены их точные значения. При сложении (или вычитании) пользуются точным значением слагаемого с наименьшим числом десятичных знаков. Остальные слагаемые округляют, оставляя после запятой одним знаком больше, чем в слагаемом с наименьшим числом знаков. В результате оставляют столько цифр после запятой, сколько их имеется в слагаемом с наименьшим числом десятичных знаков; при этом производят необходимое округление. Все расчеты производят, применяя логарифмы, пятизначные или четырехзначные. Вычисленные количества вещества отвешивают только на аналитических весах.
Взвешивание проводят или на часовом стекле, или в бюксе. Отвешенное вещество высыпают в чисто вымытую мерную колбу через чистую сухую воронку небольшими порциями. Затем из промывалки несколько раз небольшими порциями воды обмывают над воронкой бнже или часовое стекло, в котором проводилось взвешивание. Воронку также несколько раз обмывают из промывалки дистиллированной водой.
Для пересыпания твердых кристаллов или порошков в мерную колбу очень удобно пользоваться воронкой, изображенной на рис. 349. Такие воронки изготовляют емкостью 3, 6, и 10 см3. Взвешивать навеску можно непосредственно в этих воронках (негигроскопические материалы), предварительно определив их массу. Навеска из воронки очень легко переводится в мерную колбу. Когда навеска пересыпается, воронку, не вынимая из горла колбы, хорошо обмывают дистиллированной водой из промывалки.
Как правило, при приготовлении точных растворов и переведении растворяемого вещества в мерную колбу растворитель (например, вода) должен занимать не более половины емкости колбы. Закрыв пробкой мерную колбу, встряхивают ее до полного растворения твердого вещества. После этого полученный раствор дополняют водой до метки и тщательно перемешивают.
Молярные растворы. Для приготовления 1 л 1 M раствора какого-либо вещества отвешивают на аналитических весах 1 моль его и растворяют, как указано выше.
Пример. Для приготовления 1 л 1 M раствора азотнокислого серебра находят в таблице или подсчитывают молекулярную массу AgNO3, она равна 169,875. Соль отвешивают и растворяют в воде.
Если нужно приготовить более разбавленный раствор (0,1 или 0,01 M), отвешивают соответственно 0,1 или 0,01 моль соли.
Если же нужно приготовить меньше 1 л раствора, то растворяют соответственно меньшее количество соли в соответствущем объеме воды.
Нормальные растворы готовят аналогично, только отвешивая не 1 моль, а 1 грамм-эквивалент твердого вещества.
Если нужно приготовить полунормальный или децинормальный раствор, берут соответственно 0,5 или 0,1 грамм-эквивалента. Когда готовят не 1 л раствора, а меньше, например 100 или 250 мл, то берут1/10 или 1/4 того количества вещества, которое требуется для приготовления I л, и растворяют в соответствующем объеме воды.

Рис 349. Воронки для пересыпания навески а колбу.
После приготовления раствора его нужно обязательно проверить титрованием соответствующим раствором другого вещества с известной нормальностью. Приготовленный раствор может не отвечать точно той нормальности, которая задана. В таких случаях иногда вводят поправку.
В производственных лабораториях иногда готовят точные растворы «по определяемому веществу». Применение таких растворов облегчает расчеты при анализах, так как достаточно умножить объем раствора, пошедший на титрование, на титр раствора, чтобы получить содержание искомого вещества (в г) во взятом для анализа количестве какого-либо раствора.
Расчет при приготовлении титрованного раствора по определяемому веществу ведут также по грамм-эквиваленту растворяемого вещества, пользуясь формулой:

Пример. Пусть нужно приготовить 3 л раствора марганцовокислого калия с титром по железу 0,0050 г/мл. Грамм-эквивалент KMnO4 равен 31,61., а грамм-эквивалент Fe 55,847.
Вычисляем по приведенной выше формуле:

Стандартные растворы. Стандартными называют растворы с разными, точно определенными концентрациями, применяемые в колориметрии, например растворы, содержащие в 1 мл 0,1, 0,01, 0,001 мг и т. д. растворенного вещества.
Кроме колориметрического анализа, такие растворы бывают нужны при определении рН, при нефелометрических определениях и пр. Иногда стандартные растворы» хранят в запаянных ампулах, однако чаще приходится готовить их непосредственно перед применением. Стандартные растворы готовят в объеме не больше 1 л, а ча ще — меньше. Только при большом расходе стандартного раствори можно готовить несколько литров его и то при условии, что стандартный раствор не будет храниться длительный срок.
Количество вещества (в г), необходимое для получения таких растворов, вычисляют по формуле:

Пример. Нужно приготовить стандартные растворы CuSO4 • 5H2O для колориметрического определения меди, причем в 1 мл первого раствора должно содержаться 1 мг меди, второго — 0,1 мг, третьего —0,01 мг, четвертого — 0,001 мг. Вначале готовят достаточное количество первого раствора, например 100 мл.
В данном случае Mi = 249,68; АСu = 63,54; следовательно, для приготовления 100 мл раствора, 1 мл которого содержал бы 1 мг меди (Т = 0,001 г/мл), нужно взять

Навеску соли переносят в мерную колбу емкостью 100 мл и добавляют воду до метки. Другие растворы готовят соответствующим разбавлением приготовленного.
Эмпирические растворы. Концентрацию этих растворов чаще всего выражают в г/л или г/мл. Для приготовления эмпирических растворов применяют очищенные перекристаллизацией вещества или реактивы квалификации ч. д. а. или х. ч.
Пример. Нужно приготовить 0,5 л раствора CuSO4, содержашего Cu 10 мг/мл. Для приготовления раствора применяют CuSO4 • 5H2O.
Чтобы подсчитать, сколько следует взять этой солн для приготовления раствора заданного объема, подсчитывают, сколько Cu должно содержаться в нем. Для этого объем умножают на заданную концентрацию, т. е.
500*10 = 5000 мг, или 5,0000 г
После этого, зная молекулярный вес соли, подсчитывают нужное количество ее:

На аналитических весах отвешивают в бюксе точно 19,648 г чистой соли, переводят ее в мерную колбу емкостью 0,5 л. Растворение проводят, как указано выше.
Источник
Методика приготовления реактивов для проведения лабораторных работ по органической химии.
Аммиачный раствор оксида меди (I). К раствору 1 г медного купороса в 50 мл воды прибавляют 4 мл концентрированного раствора аммиака, затем раствор 3 г солянокислого гидроксиламина в 50 мл воды и хорошо перемешивают. Полученный раствор можно хранить несколько дней в хорошо закрытой склянке (в темноте). Срок хранения можно увеличить, добавив в раствор медную стружку.
Раствор можно приготовить другим способом. Для этого предварительно готовят два раствора: а) 1,5 г хлорида меди (П) и 3 г хлорида аммония растворяют в 20 мл концентрированного раствора аммиака и добавляют воды до общего объема 50 мл; б) 5 г солянокислого гидроксиламина растворяют в 50 мл воды. Перед употреблением растворы (а) и (б) смешивают в объемном соотношении 1 : 2.
Аммиачный раствор оксида серебра. К 100 мл 0,1 н. раствора нитрата серебра добавляют 0,5 мл 25%-ного раствора аммиака. Полученный раствор хранят в темной склянке не более 1 месяца. По истечении этого срока реактив, если он полностью не израсходован, осторожно нейтрализуют азотной кислотой и готовят новую порцию. Нельзя допускать испарения реактива и готовить его впрок в больших количествах.
Аммиачный раствор хлорида меди (I). 25 г кристаллического сульфата меди (II) растворяют при нагревании в 80 мл воды. К раствору прибавляют 14 г хлорида натрия. К смеси медленно при перемешивании доливают раствор 12,6 г кристаллического сульфита натрия в 20 мл воды. Смеси дают охладиться, затем промывают белый осадок хлорида меди (I) водой (декантацией), растворяют его в 30—40 мл концентрированного раствора аммиака и добавляют 200 мл воды. Бесцветный раствор хранят в плотно закрывающейся склянке над очищенной медной проволокой.
Анилин. Для очистки перегоняют (т. кип. 184 °С) с воздушным холодильником из колбы Вюрца, в которую добавляют 0,5—1 г цинковой пыли. Полученную бесцветную жидкость со слабым запахом хранят в плотно закрытой склянке (желательно заполненной почти до пробки). Добавка небольшого количества цинковой пыли стабилизирует анилин.
Анилиновая вода. Для проведения опытов по экстракции анилина его перемешивают с водой в объемном соотношении 1 : 20 и оставляют, не разделяя слои. Для исследования химических свойств анилина достаточно его растворить в воде в объемном соотношении 1 : 100.
Баритовая вода, насыщенный раствор. 70 г кристаллического гидро-ксида бария Ва (ОН)2 • 8Н20 растворяют при кипячении в 200 мл воды. Затем разбавляют водой до 1 л и дают отстояться. Через несколько часов прозрачный раствор осторожно сливают.
Бензол. Бензол марки ч. д. а. достаточно чист для большинства работ. Для удаления следов воды бензол перегоняют, отбрасывая первые 10—20% дистиллята. Т. кип. 80,2 °С.
Бром, раствор в хлороформе или тетрахлориде углерода. В склянку с притертой пробкой вносят 5 мл брома (под тягой!) и осторожно добавляют 95 мл растворителя. Склянку хранят в эксикаторе. Работать с бромом нужно в резиновых перчатках и защитных очках. Случайно разлившийся бром засыпают сульфитом или тиосульфатом натрия.
Бромид-броматная смесь. 2,8 г бромата калия в 12 г бромида калия растворяют в воде и доводят объем до 1 л (в мерной колбе).
Бромоводородная кислота. Раствор, образующийся при поглощении бромоводорода, перегоняют с дефлегматором, собирая фракцию, кипящую при 122— 126 °С. Эта фракция (р 1,47—1,49) представляет собой примерно 47%-ную бромоводородную кислоту. При перегонке сильно разбавленных растворов может получаться кислота меньшей плотности, которую при необходимости повышают повторной перегонкой. Кислоту хранят в хорошо закупоренной склянке в темноте.
Бромная вода. Для получения насыщенного раствора брома в воде в склянку с притертой пробкой вместимостью 1 л вносят 6 мл брома, добавляют 500 мл воды и энергично перемешивают. Небольшое количество брома при этом остается нерастворенным (при длительном хранении он исчезает). Для опытов используется раствор, разбавленный водой (1 : 2). Необходимо соблюдать меры предосторожности.
Глюкоза, 5%-ный раствор. Готовят не менее чем за 12 ч до начала работы с раствором. Раствор необходимо прокипятить.
2,4-Динитрофенилгидразин солянокислый. 0,2 г 2,4-динитрофенилгидразина растворяют при нагревании на водяной бане в 100 мл 2 н. раствора соляной кислоты.
Диэтиловый эфир, содержащий пероксиды. В склянку из белого стекла вместимостью 0,5 л помещают 100 мл диэтилового эфира. Добавляют примерно 10 мл концентрированной серной кислоты, взбалтывают смесь и ставят в светлое место (на окно). Ежедневно встряхивают склянку и открывают пробку для доступа воздуха. Через 8—10 дней в эфире можно обнаружить гидропероксид и уксусный альдегид. На склянке делают надпись «Диэтиловый эфир, загрязненный пероксидом. Осторожно!».
Железа (III) хлорид, 0,1 н. раствор. 9 г FeCl3 ∙6H2О растворяют в 1 л воды. При помутнении добавляют несколько капель концентрированной соляной кислоты. Банку с кристаллическим хлоридом железа необходимо снова залить парафином.
Известь натронная. Насыщенный раствор гидроксида натрия перемешивают с негашеной известью (массовое отношение 2 : 1), выпаривают досуха в железном сосуде, затем прокаливают при температуре около 500 °С и измельчают. Препарат хранят в плотно закупоренных банках. Готовую натронную известь перед использованием высушивают при 115 °С (при значительном содержании карбонатов прокаливают в муфельной печи).
Иода раствор в иодиде калия (раствор Люголя). 6 г иодида калия растворяют в 6 мл воды, размешивают в этом растворе 2 г иода и разбавляют водой до 100 мл.
Известковая вода. Гашеную известь (гидроксид кальция) перемешивают с водой. Хранят вместе с нерастворенным остатком, чтобы раствор был насыщен гидроксидом кальция. Перед использованием прозрачный раствор сливают с осадка в небольшие склянки.
Иод крахмальная бумага. 0,5 г крахмала тщательно перемешивают с 10 мл холодной воды. Полученную массу вливают в 100 мл кипящей воды и продолжают кипячение до образования однородного клейстера. После охлаждения добавляют 0,5 г иодида калия и 0,5 г кристаллического карбоната натрия, растворенных в небольшом количестве воды. Полученным раствором пропитывают фильтровальную бумагу и сушат ее на воздухе, избегая попадания солнечных лучей. Высушенную бумагу режут на полоски и хранят в плотно закрытых банках.
Калия гидроксид, 0,5 н. спиртовой раствор. Этиловый спирт кипятят 30 мин с гидроксидом калия (10 г КОН в 1 л спирта) в колбе с обратным холодильником, а потом спирт перегоняют (над той же щелочью). Затем в этот спирт при перемешивании добавляют 30—35 г гидроксида калия и через сутки быстро сливают прозрачную жидкость с осадка. Раствор хранят в темной склянке с хлоркальциевой трубкой, заполненной натронной известью.
Калия карбонат (поташ). Перед использованием прокаливают при 200 °С.
Калия перманганат, кислый раствор. К 100 мл 1%-ного раствора перманганата калия осторожно при перемешивании добавляют 5 мл концентрированной серной кислоты.
Кальция карбид. Технический продукт разбивают молотком на кусочки размером около 3—5 мм. Продукт обычно хранят в банке, залитой парафином.
Кальция хлорид. Отработанный хлорид кальция регенерируют, расплавляя его на железном противне. Слой должен быть не толще 2 см (пары воды, испаряясь, вызывают разбрызгивание, особенно большое, если слой соли толстый). После испарения всей воды нагревание продолжают еще некоторое время (при температуре 250—300 °С). Спекшуюся соль разбивают на куски и еще теплой кладут в сухую банку. Для заполнения хлоркальциевых трубок используют кусочки размером 2—5 мм.
Конго красный. Готовят 0,1%-ный раствор в воде. Раствор конго красного (для крашения). Растворяют 1 г конго красного,1 г карбоната натрия и 10 г сульфата натрия в 400 мл воды.
Крахмал, 1%-ный раствор. 1 г сухого крахмала взбалтывают с 5 мл воды, после отстаивания воду сливают. Промывание крахмала повторяют 2—3 раза. Добавив новую порцию воды, взмучивают крахмал и выливают при помешивании в 100 мл кипящей воды
Крахмальный клейстер. 2 г растворимого крахмала смешивают с 10 мл холодной воды и вливают эту кашицу в 100 мл кипящей воды. Кипятят 5—10 мин, охлаждают, дают отстояться и, если образуется хлопьевидный осадок, сливают с него раствор (или фильтруют). Для стабилизации добавляют 0,1 г КОН или салициловой кислоты (можно также 0,01 г иодида ртути).
Лактоза, 1%-ный раствор. После приготовления кипятят несколько минут.
Меди сульфат (безводный). Медный купорос нагревают в фарфоровой или никелевой чаше на песчаной бане при постоянном перемешивании. Если температура не превышает 220 °С, получается белый или слегка желтоватый продукт (при нагревании свыше 220 °С сульфат меди частично разлагается, приобретая серый цвет; при этом осушающая способность понижается). Высушенный сульфат меди растирают в ступке и хранят в сухой, плотно закрытой банке.
Меди (I) хлорид. Реактив можно приготовить двумя способами: а) 25 г медного купороса и 65 г хлорида натрия растворяют при нагревании в 80 мл воды, фильтруют, а затем к фильтрату добавляют раствор 7 г кристаллического сульфита натрия (или 3,5 г безводного) в 40 мл воды. С выпавшего осадка сливают воду и несколько раз промывают (декантацией) 2 н. раствором соляной кислоты до исчезновения сульфатиона (проба с хлоридом бария), а затем спиртом. Соль сушат при 100 °С и хранят в плотно закрытых банках. Препарат очень чувствителен к окислению. Позеленевший препарат, содержащий основные соли меди (П), вновь светлеет при промывке раствором ОД н. соляной кислоты;
б) к насыщенному раствору хлорида меди (II) добавляют кусочки меди. В склянке, которую оставляют плотно закрытой на несколько дней, постепенно выпадает белый осадок. Металлическую медь выбирают пластмассовым пинцетом, а осадок обрабатывают, как описано выше.
Метиловый красный (метилрот). 0,1 г красителя растворяют в 30 мл этанола, затем добавляют воду до 50 мл. Получают 0,2%-ный раствор индикатора. Переход от красного цвета к желтому происходит при рН= 4,2-6,2.
Метиловый оранжевый. 0,1 г индикатора растворяют в 100 мл воды.
Натрий металлический. Банку с натрием распаивают с помощью паяльника, натрий режут на куски (работать в резиновых перчатках!) и помещают их в банку с керосином или вазелиновым маслом (можно также использовать ксилол, декалин, тетралин). Для работы куски натрия извлекают из-под керосина пинцетом, быстро осушают фильтровальной бумагой и сухим ножом отрезают кусочек нужной величины. Остальную часть снова помещают в банку. С отрезанного кусочка тщательно удаляют фильтровальной бумагой следы керосина, срезают тонкие корочки, а обрезки помещают в банку с натрием. Брать натрий нужно только пинцетом. Ни в коем случае нельзя работать с натрием поблизости от водопроводного крана.
Натрия ацетат (безводный). Кристаллическую соль CH3COONa-3H20 нагревают в фарфоровой или никелевой чашке. Соль плавится в кристаллизационной воде, а по испарении большей части воды застывает. Усиливая нагревание, снова доводят соль до плавления (т. пл. 324 °С). При этом следует избегать сильного перегрева (может начаться разложение). Расплавленную соль выливают на металлическую пластинку с загнутыми краями и после остывания (теплую) измельчают в фарфоровой ступке. Хранят в плотно закрытой банке.
Натрия гидроксид (спиртовой раствор). 30 г гидроксида натрия растворяют в 30 мл воды. После охлаждения раствора добавляют этанол (ректификат) до 200 мл.
Натрия гидросульфит (натрия бисульфит) NaHS03. Гидрокарбонат или кристаллический карбонат натрия заливают водой так, чтобы она чуть покрывала кристаллы, и пропускают диоксид серы до почти полного растворения кристаллов. Полученный зеленовато-желтый раствор хранят в склянке с притертой пробкой. Диоксид серы получают, добавляя по каплям серную кислоту к сульфиту натрия в колбе Вюрца с высоким отводом. В отвод желательно вложить стекловату для задержки уносимых током газа следов жидкости. В лабораториях бывает гидросульфит натрия технический — белый слеживающийся порошок со слабым запахом сернистого ангидрида. Он обладает сильными восстанавливающими свойствами даже после длительного хранения, но истинным гидросульфитом не является. Его формула Na2S2О4 ∙2H2О, а правильное название дитионит натрия. С ацетоном и альдегидами осадков не образует.
Натрия гидроксид, 2 н. раствор. 84 г едкого натра (из расчета, что в нем 95% основного вещества) растворяют при перемешивании в 500 мл воды и доводят объем до 1 л.
Натрия сульфат (безводный). Реактив высушивают при 200—300 °С. Возможна регенерация отработанного осушителя.
n-Нитрофенилдиазонийхлорид (раствор). В стакане смешивают 12,5 мл концентрированной соляной кислоты и 150 мл воды и растворяют при нагревании 7 г п-нитроанилина. Раствор охлаждают в воде со льдом до 0 0 С и затем быстро при энергичном перемешивании приливают охлаж
денный раствор 3,5 г нитрита натрия в 20 мл воды. Реакционную смесь
оставляют в ледяной воде на 30—40 мин. Раствор диазотированного
п -нитроанилина (желтого цвета) должен быть прозрачным. В холодиль
нике он может храниться в течение 10—12 дней.
Нитрующая смесь. Смешивают 2 объема концентрированной азотной кислоты (р 1,42 г/см3) с 3 объемами концентрированной серной кислоты (р 1,84 г/см3), медленно добавляя серную кислоту к азотной при охлаждении и перемешивании.
Орциновый реактив. 1 г орцина растворяют в 500 мл 25%-ного раствора соляной кислоты и добавляют 20 капель 3%-ного раствора хлорида железа (III).
Реактив Селиванова. 50 мл концентрированной соляной кислоты смешивают с 50 мл воды. В 100 мл полученного раствора соляной кислоты (1:1) растворяют 0,5 г резорцина. Используют в реакциях накетогексозы.
Реактив Толленса. К 20 мл 5%-ного раствора нитрата серебра прибавляют 10 мл 10%-ного раствора гидроксида натрия. К выпавшему осадку оксида серебра добавляют 5 мл разбавленного раствора аммиака (10 мл концентрированного раствора аммиака разбавляют 100 мл дистиллированной воды). Колбу закрывают пробкой и встряхивают. Повторяют операцию до полного растворения осадка, избегая избытка аммиака. Затем добавляют воду до объема 100 мл.
Сахароза, 1%-ный раствор. Растворяют 10 г сахарозы (или пищевого сахара) в 1 л воды, фильтруют и кипятят несколько минут.
Серебра нитрат, 0,2 н. раствор. 3,4 г нитрата серебра растворяют в 20 мл воды и доводят объем до 100 мл. Для приготовления раствора используется бидистиллят. Посуда должна быть очень тщательно отмыта от возможных органических загрязнений. Хранят раствор в темной склянке с притертой пробкой.
Серебра остатки, регенерация. Все растворы и осадки, содержащие серебро, подлежат сбору и переработке. Ацетиленид серебра и «серебряное зеркало» растворяют в разбавленной азотной кислоте.
К остаткам серебра прибавляют раствор гидроксида натрия до щелочной реакции по фенолфталеину, нагревают на водяной бане и добавляют формалин. Через 5—15 мин выделяется темно-серый рыхлый порошок металлического серебра. Его отсасывают, промывают водой до удаления щелочи и хлорид-ионов и сушат при 100 °С. К навеске высушенного осадка прибавляют избыток азотной кислоты (1 мл азотной кислоты плотностью 1,42 г/см3 или 1,5 мл плотностью 1,31 г/см3 на 1 г серебра) и нагревают при 50 °С до растворения. Жидкость фильтруют и упаривают на водяной бане до появления кристаллической пленки. Если за это время оксиды азота не удалились полностью, добавляют воду и упаривают вновь. Упаренный раствор охлаждают, кристаллы нитрата серебра отсасывают, промывают небольшим количеством ледяной воды и сушат при 110 °С. Маточный раствор и промывные воды можно упарить и выделить дополнительное количество нитрата серебра или же слить в склянку с остатками серебра.
Серная кислота 2 н. 56 мл концентрированной серной кислоты (р 1,84 г/см 3 ) медленно прибавляют к 944 мл воды.
Соляная кислота 2 н. 167 мл концентрированной соляной кислоты (р 1,19 г/см 3 ) разбавляют водой до 1 л.
Углеводороды насыщенные жидкие. Образцом смеси жидких предельных углеводородов может служить петролейный эфир (tкип
+60 °С), который представляет собой смесь углеводородов, главным образом смесь пентана и гексана. Перед работой проверяют петролейный эфир на отсутствие непредельных углеводородов реакциями с бромной водой и с раствором перманганата калия. Насыщенные жидкие углеводороды можно выделить из бензина или керосина. Для отделения насыщенных углеводородов от ненасыщенных (и от других примесей) бензин (или керосин) обрабатывают 3—4 раза концентрированной серной кислотой в делительной воронке (на 100 мл бензина или керосина берут 10 мл серной кислоты). Вначале углеводороды с серной кислотой встряхивают осторожно, затем, когда смесь перестанет разогреваться, сильно. Пары и газы выпускают, как обычно, приоткрывая кран (воронка в этот момент должна быть перевернута краном вверх). Обработку углеводородов каждой порцией серной кислоты ведут в течение 5—10 мин. После серной кислоты углеводороды обрабатывают в той же делительной воронке 1%-ным раствором перманганата калия, к которому добавлен 5%-ный раствор карбоната натрия. В заключение их промывают водой. После отделения воды (нижнего слоя) углеводороды сливают в колбу и сушат гранулированным хлоридом кальция. Приготовленная таким способом смесь углеводородов состоит из алканов и циклопарафинов (нафтенов), которые по многим свойствам похожи на алканы; в приведенных в практикуме опытах присутствие циклопарафинов не обнаруживается.
Углеводороды ненасыщенные жидкие. Для опытов с жидкими ненасыщенными углеводородами можно использовать бензин или керосин: в них содержится некоторое количество смеси алкенов. Больше всего алкенов в крекинг-бензине. Если бензин (керосин) не бесцветен, его перегоняют, собирая бесцветный дистиллят в широких температурных пределах.
Уксусная кислота 2 н. 116 мл ледяной уксусной кислоты разбавляют водой до 1 л.
Фелингова жидкость (реактив Фелинга). Готовят два раствора. Раствор I. 34,6 г чистого перекристаллизованного сульфата меди растворяют в воде, содержащей несколько капель серной кислоты, и разбавляют до 500 мл.
Раствор II. 173 г сегнетовой соли (тартрат натрия-калия) растворяют в 200 мл воды, добавляют раствор 70 г гидроксида натрия (или 85 г гидроксида калия) в 100 мл воды и разбавляют до 500 мл.
Фелингову жидкость готовят непосредственно перед каждой лабораторной работой, смешивая равные объемы растворов I и П (исходные растворы могут храниться неограниченно долго).
Если отсутствует сегнетова соль, то для приготовления раствора П растворяют 121 г гидроксида натрия и 93,1 г чистой винной кислоты в 400 мл воды и доводят объем до 500 мл.
Фенилгидразин уксуснокислый (раствор). 10 г солянокислого фенил-гидразина и 20 г ацетата натрия растворяют при небольшом нагревании в 200 мл воды. Теплый раствор фильтруют. (Фенилгидразин вызывает экзему, поэтому работа с ним требует соблюдения правил техники безопасности.)
Фенолфталеин. 0,2 г фенолфталеина растворяют в 165 мл спирта и добавляют 135 мл воды.
Фишера реактив. В сухую склянку из темного стекла вносят 200 мл пиридина, растворяют в нем 100 г иода и добавляют 600 мл метанола. Склянку плотно закрывают и оставляют на двое суток. Затем склянку взвешивают и помещают в баню со льдом, а через раствор пропускают диоксид серы из баллона до увеличения массы на 45—50 г. Приготовленный таким образом реактив выдерживают перед использованием не менее недели. Хранят, хорошо защищая от влаги.
Флороглюцин (раствор). 0,4 г флороглюцина растворяют в 200 мл 30%-ной соляной кислоты.
Фруктоза, 0,5%-ный раствор. После приготовления раствор кипятят.
Фурфурол. Соломенно-желтая жидкость, быстро темнеющая на воздухе. Очищают перегонкой, собирая фракцию, кипящую при 159—163 °С (т. кип. чистого фурфурола 162 °С). Окисление (потемнение) фурфурола замедляют добавкой 0,1% гидрохинона или пирогаллола.
Фуксинсернистая кислота (раствор). 0,2 г фуксина растворяют в 200 мл дистиллированной воды и вводят 2 г гидросульфита натрия и 2 мл концентрированной соляной кислоты. Если через 15—20 мин жидкость не обесцветится, то добавляют немного активированного угля, встряхивают смесь до обесцвечивания и затем фильтруют. Реактив хранят в плотно закрывающейся склянке из темного стекла. Чем меньше избыток оксида серы (IV) в реактиве, тем он чувствительнее.
Хромовая смесь (смесь Бекмана). В 100 мл воды растворяют 20 г дихромата калия и добавляют 10 мл концентрированной серной кислоты. Такая хромовая смесь (смесь Бекмана) предназначена для окисления спиртов и анилина и не годится для мытья посуды.
Щавелевая кислота, 0,01 н. В мерной колбе вместимостью 1 л растворяют в 100 мл воды 0,63 г свежеперекристаллизованной щавелевой кислоты. Затем добавляют 1 мл 30%-ной H2S04 и разбавляют водой до метки.
Швейцера реактив (медно-аммиачный реактив). К раствору 10 г медного купороса в 100—200 мл воды добавляют 100 мл 2 н. раствора гидроксида натрия. Образовавшийся осадок отсасывают, промывают несколько раз водой до отрицательной реакции на сульфат-ион и растворяют в минимальном количестве 25%-ного раствора аммиака. Часть гидроксида меди при этом должна остаться нерастворенной. Раствору дают отстояться и сливают декантацией. Эмпирическая формула реактива [Cu(NH3)4](OH)2.
Эфир абсолютный. Эфир проверяют на наличие пероксидов, встряхивая его с равным объемом 2%-ного раствора иодида калия, подкисленного разбавленной соляной кислотой. Присутствие пероксидов определяют по синей окраске водного слоя при добавлении раствора крахмала. (Подкисленный серной кислотой раствор ванадата аммония с эфиром, содержащим пероксиды, окрашивается в красный цвет, а такой же раствор дихромата калия — в синий.)
Если пероксиды отсутствуют, приступают к осушке, если они есть, от них избавляются встряхиванием раствора с порошкообразным гидроксидом калия (70 г на 1 л).
После отстаивания эфир сливают, добавляют 100 г хлорида кальция и через сутки фильтруют. Затем в эфир вносят около 5 г металлического натрия в виде тонко нарезанных листочков или проволоки, выдавливаемой из пресса. Если через 24 ч не наблюдается выделения пузырьков водорода, то осушка считается законченной, если же водород выделяется, добавляют еще 2—3 г натрия.
Эфир можно перегнать на водяной бане над натрием, предохраняя его от атмосферной влаги, но можно обойтись и без перегонки, лишь слив его в сухую склянку. Склянку с эфиром закрывают корковой пробкой с хлоркальциевой трубкой. Для предотвращения окисления можно внести несколько крупинок дифениламина или фосфорного ангидрида, или, еще лучше, несколько гранул гидроксида калия, который действует одновременно и как осушитель.
Источник