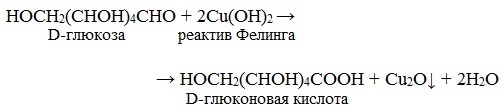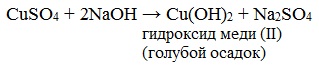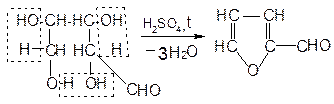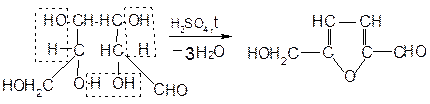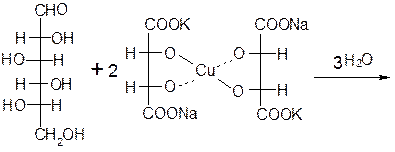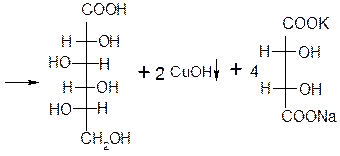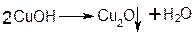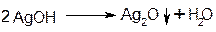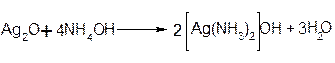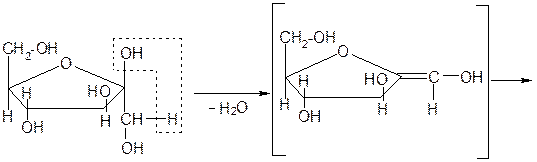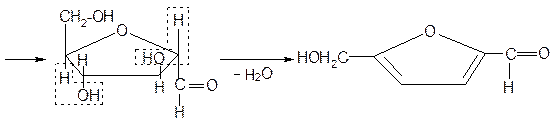ПРИГОТОВЛЕНИЕ РЕАКТИВОВ, ИСПОЛЬЗУЕМЫХ ДЛЯ ХИМИЧЕСКИХ АНАЛИЗОВ
Для химических анализов мороженого используют химически чистые реактивы. Вода для приготовления растворов реактивов и проведения определений должна быть только дистиллированной.
Реактивы для определения кислотности: децинормальный раствор едкого натра или едкого кали, 95%-ный спирт этиловый, ,1%-ный спиртовой раствор фенолфталеина, вода.
Для приготовления 1 л несколько крепче децинормального раствора едкого натра или едкого кали требуется 7 мл нормального раствора; дистиллированная вода должна быть свободна от углекислоты. Титр устанавливают по 0,1 н. раствору янтарной или щавелевой кислоты.
Раствор фенолфталеина готовят следующим образом: 1 г фенолфталеина растворяют в 70 мл 95°/о-ного этилового спирта, добавляют 30 мл воды.
Дистиллированную воду необходимо иметь свежепрокипяченную для удаления углекислоты; после кипячения воду охлаждают до комнатной температуры.
Реактивы для определения жирности: кислота серная, спирт изоамиловый плотностью 0,8108—0,8115 при 20-г4°С.
Обычно применяют техническую серную кислоту. Плотность продажной серной кислоты 1,826—1,835; для определения жирности мороженого необходима кислота плотностью 1,5—1,55. Предварительно определяют концентрацию имеющейся продажной кислоты, затем ее азвоДят Для получения кислоТы необходимой плотности, приливая кислоту в воду небольшими порциями.
Реактивы для определения содержаниясахара: Для приготовления фильтрата: натр едкий 1 н. раствор, медь сернокислая, раствор Фелинга № 1. Для приготовления раствора Фе- инга № 1 взвешивают 69,26 г свежеперекристаллизоваиной сернокислой меди с точностью до 0,1 г и растворяют в мерной колбе вместимостью до 1 л.
При йодометрическом методе определения: натр едкий, кислота соляная, калий йодистый, метиловый оранжевый, йод металлический, крахмал, калий двухромовокислый, натрий серноватистокислый. г Натр едкий используют в виде нормального и децинормального раствора, кислоту соляную—в виде 0,5 н. раствора и раствора 1:5, а также раствора для инверсии; для приготовления последнего 120 мл | соляной кислоты плотностью 1,19 помещают в мерную колбу вмести- I мостью 200 мл и доливают водой до метки.
Метиловый оранжевый используют в виде 0,1%-ного водного расBopa, крахмал — в виде 1%-ного раствора.
Йод металлический — применяют 0,1 н. раствор; для этого 20— 25 г йодистого калия, отвешенного с точностью до 1 г в стакане :: вместимостью 100 мл, растворяют в возможно малом количестве воды. В стакан с раствором прибавляют 12,7 г йода, отвешенного с точностью до 0,01 г, жидкость перемешивают до полного растворения ; йода и количественно переносят в мерную колбу вместимостью 1 л, которую затем дополняют водой до метки. Для установки титра используют 0,1 н. раствора тиосульфата (Na2S203).
Калий двухромовокислый используют в виде 0,1 н. раствора; 4,9038 г двухромовокислого калия, перекристаллизованного и высушенного при 150° С, взвешивают с точностью до 0,0002 г, переводят количественно в мерную колбу вместимостью 1 л, растворяют и до- ‘ полняют водой до метки.
Натрий серноватистокислый используют в виде 0,1 н. раствора. Приготовление и установку титра раствора производят следующим, образом. Серноватистокислый натрий в количестве 25 г отвешивают с точностью до 0,1 г, переводят в мерную колбу вместимостью 1 л, растворяют и добавляют водой до метки. В коническую колбу с притертой пробкой вместимостью 750 мл помещают 1—2 г йодистого 1 калия, растворяют его в возможно малом количестве воды, прибавляют 5 мл соляной кислоты (1 : 5) и пипеткой приливают 20 мл 0,1 н. раствора двухромовокислого .калия, и около 300 мл воды. Закрывая колбу пробкой, содержимое ее перемешивают и через 3—5 мин титруют раствором серноватистокислого натрия при помешивании. После перехода бурого цвета раствора в желтовато-зеленый приливают 1 мл раствора крахмала и титрование продолжают до перехода цве- t та раствора из синего в светло-зеленый.
При определении по методу Бертрана: калий — натрий виннокислый (химически чистый), медь сернокислая для приготовления раствора Фелинга № 1, раствор Фелинга № 2, натр едкий, кислота соляная, кислота серная плотностью 1,84, натрий щавелевокислый или аммоний щавелевокислый, квасцы железоаммонийные, метиловый оранжевый, калий марганцовокислый.
Для приготовления раствора Фелинга № 2 берут 365 г калия — натрия виннокислого (сегнетовой соли), взвешенного с точностью до 0,5 г, растворяют при слабом нагревании в 600 мл воды и фильтруют в мерную колбу вместимостью 1 л, затем в него подливают приготовленный отдельно раствор 103 г едкого натра в 200 мл воды, после чего объем раствора в колбе доводят водой до метки.
Кислоту соляную используют в виде раствора для инверсии, а метиловый оранжевый—в виде 0,1%-ного раствора.
Раствор железоаммонийных квасцов приготовляют следующим образом. К 250 мл насыщенного на холоду раствора железоаммонийных квасцов приливают 25 мл серной кислоты; раствор перемешивают, охлаждают, переводят в мерную колбу вместимостью в 1 л, разбавляют водой до горлышка колбы и после охлаждения до температуры 20° С доводят раствор водой до метки. Б момент определения раствор имеет комнатную температуру, но не менее 20° С.
1 мл раствора калия марганцовокислого должен соответствовать приблизительно 10 мг меди. Калий марганцовокислый в количестве 4,98 г, отвешенных с точностью до 0,001 г, количественно переводят в мерную колбу вместимостью в 1 л, растворяют и доводят водой до метки. Раствор фильтруют через асбестовый фильтр, предварительно промытый тем же раствором, и хранят в бутыли из темного стекла. Титр раствора устанавливают посредством навесок щавелевокислого натрия (аммония) следующим образом. Около 25 г щавелевокислого натрия (аммония) взвешивают с точностью до 0,0002 г, количественно переводят в коническую колбу и растворяют в 100 мл воды. По прибавлении в колбу 2 мл серной кислоты раствор нагревают до температуры около 80° С и титруют раствором марганцовокислого калия до появления розового окрашивания.
В изготовлении продукции здесь могут использоваться любые виды химических реактивов. С помощью таких веществ могут проводиться и разнообразные анализы, а также исследования или эксперименты.
растворы их, употребляемые при химическом анализе (см.) для определения качественного и количественного состава тел, их свойств или химической функции и химического строения. Так, напр., серная кислота представляет реактив для.
• Микрокристаллоскопия, — метод качественного химического анализа, основанный на исследовании характерных кристаллических осадков, образующихся при воздействии соответствующих реактивов на исследуемый раствор.
Химия предлагает нам целый ряд реактивов, при помощи которых мы можем узнать присутствие белковых веществ.
Таким образом, химический анализ и микроскопическое исследование идут рука об руку и взаимно пополняются.
Источник
Жидкость фелинга как приготовить
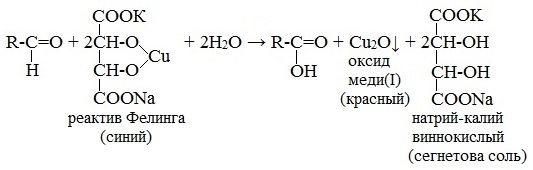
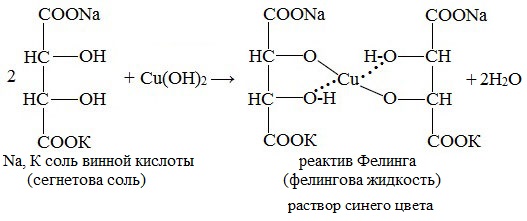
Реактив Фелинга (медно-тартратный реактив, фелингова жидкость) — состоит из равных объемов раствора сложной соли тартрата натрия-калия (сегнетова соль, натрий-калий виннокислый) в 10%-ном р-ре NaOH и раствора сульфата меди.
Приготавливается непосредственно перед анализом путем смешения двух растворов.
Применяется для качественного и количественного определения альдегидов жирного ряда и в особенности моносахаридов. Действие реактива Фелинга основано на восстановлении иона двухвалентной меди до одновалентной за счёт окисления альдегидных групп исследуемых соединений.
При этом на холоде выпадает оранжево-жёлтый осадок гидроксида меди (I) СuОН, а при нагревании – красный осадок оксида меди (I) Сu2O.
Впервые был предложен в 1850 году немецким химиком Г. Фелингом.
Реакция на моносахариды
Глюкоза окисляется свежеосажденным гидроксидом меди (II) в щелочной среде до глюконовой кислоты, восстанавливая ионы Cu +2 до Cu +1 . Углеводы подобного типа называют восстанавливающими.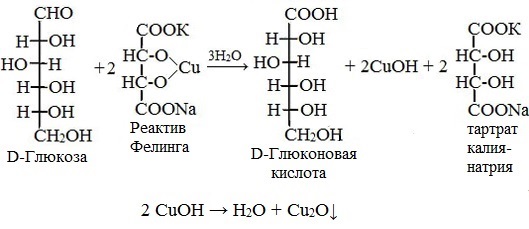
Эта реакция применяется для количественного определения сахаров в пищевых продуктах.
Реакция на альдегиды
Альдегиды жирного ряда восстанавливают двухвалентную медь в одновалентную.
Ароматические альдегиды эту реакцию не дают.
Образование реактива Фелинга
Реактив Фелинга используется как качественная реакция для определения альдегидной группы.
Источник
Приготовление реактива Фелинга (фелинговой жидкости).



УГЛЕВОДЫ.
Углеводы – важнейшие природные органические соединения, в состав которых входят карбонильная и не менее двух гидроксильных групп. По составу и строению углеводы делят на несколько групп. Простые углеводы, или моносахариды, — это вещества не способные гидролизироваться (например, глюкоза и фруктоза и др.). Углеводы состоящие из двух и более остатков моносахаридов, называются – олигосахаридами. В эту группу углеводов входят дисахариды (сахароза, лактоза и др.). Полисахариды, или полозы, состоят из большого числа остатков моносахаридов, определенным образом связанных между собой (крахмал, гликоген, клетчатка и др.).
Лабораторная работа №10.
МОНОСАХАРИДЫ.
ОПЫТ №1: Качественная реакция на углеводы с α-нафтолом (реакция Молиша).
При взаимодействии с концентрированной серной кислотой все углеводы разлагаются с образованием различных веществ, в частности фурфурола и его производных, которые конденсируются с α-нафтолом с образованием окрашенных соединений.
Реактивы и оборудование: концентрированные растворы углеводов: глюкозы (моносахарид), сахарозы (дисахарид) и крахмала (полисахарид), 15% спиртовой раствор α-нафтолола, концентрированная серная кислота; пипетки, пробирки.
Ход работы: В три пробирки наливают по 1 мл концентрированных раствора углеводов. В первую – глюкозу, во вторую – сахарозы и в третью – крахмал. Во все пробирки добавляют по 2-3 капли 15% спиртового раствора α-нафтола, а затем осторожно по стенке при помощи пипетки приливают по 1 мл концентрированной серной кислоты. Серная кислота опускается на дно пробирки, и на границе двух слоев постепенно образуется кольцо красно-фиолетового цвета.
Схема образования фурфурола и оксиметилфурфурола:
ОПЫТ №2: Окисление моносахаридов реактивом Фелинга.
Реактивом Фелинга легко окисляются как альдозы, так и кетозы, но следует отметить, что в реакцию с данным реактивом вступают не сами кетозы, а продукты их щелочной деструкции в присутствии окислителя.
Приготовление реактива Фелинга (фелинговой жидкости).
Готовят два раствора: а) 34,6 г кристаллического сульфата меди в 500 мл воды; б) 173 г сегнетовой соли (натриво-калиевая соль винной кислоты), 70 г гидроксида натрия в 500 мл воды. Перед употреблением смешивают равные объемы этих растворов.
Реактивы и оборудование: 1% раствор глюкозы, 1% раствор фруктозы, реактив Фелинга; спиртовки, пипетки, пробирки.
Ход работы: В две пробирки по 1 мл 1% раствора глюкозы 1% раствора фруктозы. В обе пробирки добавляют по 1 мл реактива Фелинга. Содержимое пробирок тщательно перемешивают и нагревают верхнюю часть раствора до начинающегося кипения. В обоих случаях в верхней части раствора появляется желтый осадок гидроксида меди (I), переходящий в красно-оранжевый осадок оксида меди (I). Цвет нижней части пробирок остается неизменным.
D-глюкоза реактив Фелинга
Реактивом Фелинга пользоваться удобнее, чем гидроксидом меди (II), так как при нагревании этого реактива с раствором моносахарида не происходит образование черного осадка оксида меди (II), маскирующего красно-оранжевый цвет осадка оксида меди (I). К тому же реакция с фелинговой жидкостью протекает быстрее, поэтому ее широко используют для качественного и количественного определения моносахаридов.
ОПЫТ №3: Окисление моносахаридов аммиачным раствором гидроксида серебра (реакция ″серебряного зеркала″).
Реактивы и оборудование: аммиачный раствор серебра, 1% раствор глюкозы, 1% раствор фруктозы; водяная баня, пипетки, пробирки.
Приготовление аммиачного раствора серебра.
К 1% раствору нитрата серебра при встряхивании по каплям прибавляют 5% раствор аммиака до тех пор, пока образовавшийся в начале осадок полностью не раствориться:
Ход работы: В двух чистых пробирках готовят по 2 мл аммиачного раствора серебра. В первую добавляют 1,5 мл 1% раствора глюкозы, во вторую 1,5 мл 1% фруктозы. Пробирки ставят на водяную баню при 70-80˚ С на 10-15 минут. Металлическое серебро выделяется и оседает на стенках обеих пробирок. Следует помнить, что при нагревании пробирки нельзя трогать и встряхивать, иначе серебро выпадет в виде черного осадка.

ОПЫТ №4: Реакция Селиванова на кетогексозы.
Реактивы и оборудование: 2% раствор глюкозы, 2% раствор фруктозы, насыщенный раствор меда, реактив Селиванова; водяная баня, пипетки, пробирки.
Приготовление реактива Селиванова:
50 мл концентрированной соляной кислоты смешивают с 50 мл воды, к полученному раствору добавляют 0,5 г резорцина.
Ход работы: В три пробирки наливают по 2 мл реактива Селиванова. В первую добавляют 3-4 капли 2% раствора фруктозы, во вторую столько же раствора меда, в третью – глюкозы. Пробирки ставят на водяную баню при 80˚ С на 5-10 минут. В пробирке с фруктозой появляется оранжевое, переходящее в розово-красное окрашивание. Раствор, содержащий глюкозу, не окрашивается. Так как натуральный мед состоит преимущественно из фруктозы, в пробирке с его раствором так же развивается розово-красное окрашивание. Этот опыт может служить проверкой натуральности меда.
Эта реакция позволяет различить альдозы и кетозы. При нагревании с соляной кислотой фруктоза (кетоза) превращается в оксиметилфурфурол, который вступает в реакцию конденсации с резорцином, в результате чего получается соединение окращенное в розово-красный цвет. Альдозы так же дают эту реакцию, но протекает она гораздо медленнее и при длительном кипячении.
Источник